Дата поступления рукописи в редакцию: 05.01.2025 г.
Дата принятия рукописи в печать: 14.01.2025 г.
Date of receipt of the manuscript by the editorial office: 05.01.2025
Date of acceptance of the manuscript for publication: 14.01.2025
ВВЕДЕНИЕ
Травма крестообразной связки (ТКС) представляет собой одно из наиболее распространенных и серьезных повреждений коленного сустава, значительно влияющих на функциональность и качество жизни пациентов [1, 2]. В современной спортивной медицине и травматологии продолжается дискуссия о наиболее эффективных методах лечения данной патологии, что обусловливает высокую актуальность исследований в этой области [3, 4]. Традиционно подходы к лечению ТКС разделяются на хирургические и консервативные, каждый из которых имеет свои преимущества и ограничения [5–7].
Хирургическое вмешательство, в частности артроскопическая реконструкция связки, долгое время считалось золотым стандартом лечения, особенно для молодых и физически активных пациентов. Этот метод позволяет восстановить анатомическую целостность связки и, теоретически, обеспечить более полное восстановление функции колена [2, 8]. С другой стороны, консервативное лечение, основанное на интенсивной физиотерапии и реабилитации, приобретает все большую популярность благодаря меньшей инвазивности и потенциально меньшему риску осложнений [9, 10].
Однако, несмотря на значительный прогресс в обоих направлениях, остается ряд нерешенных вопросов, касающихся долгосрочных результатов лечения, влияния выбранного метода на качество жизни пациентов и оптимальных критериев выбора тактики лечения для каждого конкретного случая. Особый интерес представляет изучение психологических аспектов восстановления после ТКС, которые до настоящего времени оставались недостаточно изученными в контексте сравнения различных методов лечения [1–19].
Цель данного исследования заключается в проведении сравнительного анализа хирургических и консервативных методов лечения травмы крестообразной связки с особым акцентом на долгосрочные результаты и качество жизни пациентов. Более того, в рамках данной работы предлагается подход, интегрирующий психологическую реабилитацию в процесс лечения ТКС, что потенциально может улучшить как краткосрочные, так и отдаленные результаты терапии.
МАТЕРИАЛ И МЕТОДЫ
Передняя крестообразная связка (ПКС) представляет собой ключевой стабилизатор коленного сустава, играющий критическую роль в его биомеханике [11]. Глубокое понимание анатомии, функций и механизмов травмирования ПКС является фундаментальным для разработки эффективных стратегий лечения и реабилитации.
Анатомически ПКС представляет собой внутрисуставную, но экстрасиновиальную структуру, состоящую преимущественно из плотной соединительной ткани. Связка берет начало от заднемедиальной поверхности латерального мыщелка бедренной кости, проходит косо через межмыщелковую ямку и прикрепляется к переднемедиальной части межмыщелкового возвышения большеберцовой кости [9, 12, 13]. Средняя длина ПКС варьируется от 31 до 38 мм, а ширина составляет 10–12 мм, однако эти параметры могут значительно различаться у разных индивидуумов (рис. 1).
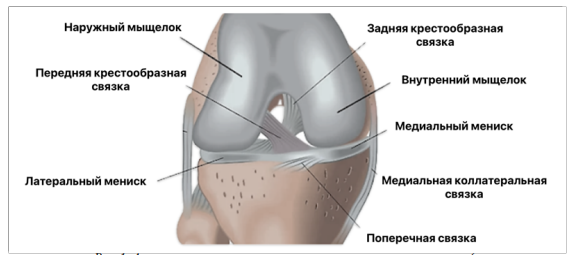
Рис. 1. Анатомическое строение коленного сустава человека (составлена автором на основе [20])
Микроструктура ПКС характеризуется сложной организацией коллагеновых волокон, преимущественно типа I [14]. Эти волокна объединены в пучки, окруженные рыхлой соединительной тканью — эндотеноном. Группы пучков формируют фасцикулы, окруженные эпитеноном [6]. Такая иерархическая организация обеспечивает высокую прочность связки и ее способность противостоять многонаправленным нагрузкам.
ПКС традиционно рассматривается как состоящая из двух функциональных пучков:
1. Антеромедиальный пучок (AM) — более длинный и тонкий, расположен в переднемедиальной части связки. Он натягивается при сгибании колена и играет ключевую роль в ограничении переднего смещения большеберцовой кости в положении сгибания.
2. Постеролатеральный пучок (PL) — более короткий и толстый, расположен сзади и латерально. Этот пучок натягивается при разгибании колена и обеспечивает ротационную стабильность, особенно при небольших углах сгибания [9].
Однако современные исследования указывают на более сложную структурную организацию ПКС. Некоторые авторы выделяют третий, промежуточный пучок, а другие рассматривают ПКС как континуум волокон с различными функциональными характеристиками, а не как четко разделенные пучки.
Кровоснабжение ПКС осуществляется преимущественно за счет средней коленной артерии, ветви подколенной артерии. Дополнительное кровоснабжение обеспечивается нижними коленными артериями. Важно отметить, что центральная часть связки имеет относительно бедное кровоснабжение, что может влиять на процессы заживления и регенерации при повреждениях [14, 15].
Иннервация ПКС осуществляется ветвями большеберцового нерва. В структуре связки обнаружены различные типы механорецепторов:
1. Тельца Руффини — медленно адаптирующиеся рецепторы, реагирующие на растяжение.
2. Тельца Пачини — быстро адаптирующиеся рецепторы, чувствительные к ускорению и замедлению движений.
3. Сухожильные органы Гольджи — реагирующие на изменения напряжения в связке.
4. Свободные нервные окончания — отвечающие за ноцицепцию.
Эта сложная сенсорная система играет ключевую роль в проприоцепции и нейромышечном контроле коленного сустава.
Функции ПКС многогранны и включают:
1. Ограничение переднего смещения большеберцовой кости относительно бедренной — основная механическая функция, обеспечивающая до 86 % сопротивления переднему смещению при углах сгибания 30–90 °.
2. Контроль ротационной стабильности колена — ПКС ограничивает внутреннюю ротацию голени, особенно в сочетании с вальгусной нагрузкой.
3. Вторичная стабилизация при вальгусных и варусных нагрузках — ПКС работает совместно с коллатеральными связками для обеспечения фронтальной стабильности колена.
4. Проприоцептивная функция — механорецепторы в ПКС обеспечивают обратную связь о положении и движении сустава, что критически важно для нейромышечного контроля и координации движений.
5. Направление движения суставных поверхностей — ПКС участвует в регуляции феномена «roll-back» мыщелков бедра по плато большеберцовой кости при сгибании колена.
Механизмы травмирования ПКС разнообразны, но можно выделить несколько основных типов [1–3]:
1. Неконтактный механизм (70– 80 % случаев):
• резкое замедление с последующим изменением направления движения, часто наблюдаемое в спортивных играх;
• приземление после прыжка на выпрямленную или почти выпрямленную ногу с последующим вальгусным отклонением колена;
• гиперэкстензия колена, часто в сочетании с ротацией голени.
2. Контактный механизм (20–30 % случаев):
• прямой удар по колену, особенно с латеральной стороны, вызывающий вальгусное отклонение и внешнюю ротацию голени;
• форсированное сгибание колена при фиксированной стопе.
3. Комбинированный механизм:
• Наиболее опасная комбинация включает вальгусное отклонение, внутреннюю ротацию бедра и внешнюю ротацию голени при частично согнутом колене. Это положение создает максимальное напряжение в ПКС, часто превышающее ее прочностные характеристики.
Биомеханические исследования показывают, что ПКС способна выдерживать нагрузки до 2000 Н при изолированном растяжении. Однако в условиях комплексных нагрузок, особенно при сочетании сдвиговых и ротационных сил, разрыв может произойти при значительно меньших нагрузках [7, 16].
Важно отметить, что существуют значительные индивидуальные различия в анатомии и биомеханике ПКС. Факторы риска травмирования включают:
• анатомические особенности (узкая межмыщелковая вырезка, повышенный задний наклон большеберцового плато);
• гормональные факторы (влияние эстрогенов на свойства связок у женщин);
• нейромышечный контроль и паттерны движений;
• генетическая предрасположенность.
Понимание этих нюансов анатомии, функций и механизмов травмирования ПКС имеет критическое значение для разработки эффективных стратегий профилактики, оптимизации хирургических техник реконструкции и создания индивидуализированных протоколов реабилитации. Современные подходы к лечению травм ПКС учитывают не только механическую функцию связки, но и ее роль в проприоцепции и нейромышечном контроле коленного сустава, что отражается в комплексных программах реабилитации, включающих как физические, так и нейрокогнитивные аспекты восстановления [3, 4].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Сравнительный анализ хирургических и консервативных методов лечения
Сравнительный анализ хирургических и консервативных методов лечения травмы крестообразной связки (ТКС) представляет собой ключевой аспект в определении оптимальной стратегии ведения пациентов [4, 12]. Каждый подход имеет свои преимущества и недостатки, которые необходимо тщательно оценить для принятия обоснованного клинического решения [10].
Хирургические методы лечения ТКС, основанные на артроскопической реконструкции связки, представляют собой сложную и высокотехнологичную процедуру. Современные техники реконструкции стремятся к максимально точному воспроизведению нативной анатомии и биомеханики ПКС (рис. 2). Это достигается путем тщательного позиционирования костных каналов и выбора оптимального трансплантата [11, 17].
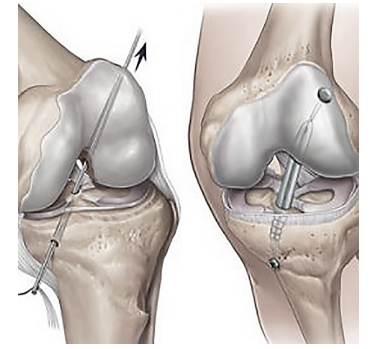
Рис. 2. Техника артроскопической реконструкции передней крестообразной связки (ПКС) коленного сустава трансплантатом (составлена автором на основе [21])
Использование аутотрансплантатов, таких как связка надколенника или сухожилия подколенных мышц, имеет свои нюансы. Связка надколенника обеспечивает более быструю интеграцию за счет костных блоков на концах трансплантата, но может вызывать длительный дискомфорт в передней части колена. Сухожилия полусухожильной и нежной мышц позволяют создать многопучковый трансплантат, лучше имитирующий структуру нативной ПКС, однако требуют более длительного периода врастания в костные каналы [8, 9, 13].
Аллотрансплантаты, хотя и исключают травматизацию донорского места, имеют более медленную биологическую интеграцию и потенциально больший риск растяжения со временем. Выбор между ауто- и аллотрансплантатом часто зависит от возраста пациента, уровня физической активности и сопутствующих заболеваний.
Артроскопическая техника позволяет не только восстановить механическую функцию связки, но и минимизировать повреждение проприоцептивных структур сустава. Это критически важно для восстановления полноценной функции колена, включая нейромышечный контроль и координацию движений [5, 6, 17].
Успех реконструкции зависит от множества факторов, включая точность позиционирования трансплантата, его натяжение и фиксацию, а также последующую биологическую интеграцию. Современные методики направлены на оптимизацию каждого из этих аспектов для достижения максимально возможного функционального результата [18, 19].
В свою очередь консервативные методы лечения ТКС представляют собой комплексный подход, основанный на глубоком понимании биомеханики коленного сустава и нейромышечной регуляции движений [1–3]. Интенсивная физиотерапия и реабилитация без хирургического вмешательства направлены на создание функционального «динамического стабилизатора» колена, компенсирующего отсутствие механической стабильности, обеспечиваемой интактной ПКС.
Комплекс упражнений, применяемых при консервативном лечении, тщательно структурирован и прогрессирует от изометрических упражнений в закрытой кинетической цепи до сложных плиометрических и спорт-специфичных движений. Особое внимание уделяется не только укреплению четырехглавой мышцы бедра и задней группы мышц бедра, но и тренировке мышц-стабилизаторов тазобедренного сустава и корпуса, играющих ключевую роль в контроле положения нижней конечности при динамических нагрузках [5, 11].
Улучшение проприоцепции достигается через прогрессивные упражнения на баланс и координацию, включая использование нестабильных поверхностей и виртуальной реальности. Эти методики направлены на восстановление нейромышечного контроля и адаптацию центральной нервной системы к измененной биомеханике колена.
Современные методы физиотерапии, такие как электромиостимуляция с биологической обратной связью, позволяют целенаправленно воздействовать на отдельные мышечные группы, ускоряя их восстановление и улучшая нервно-мышечную координацию. Криотерапия применяется не только для уменьшения боли и отека, но и для модуляции воспалительного ответа и оптимизации процессов регенерации тканей. Гидрокинезотерапия обеспечивает возможность ранней нагрузки в условиях сниженной гравитации, что особенно важно для восстановления проприоцепции и нормальных паттернов движения.
Использование ортезов при консервативном лечении ТКС эволюционировало от простой иммобилизации к функциональным брейсам с динамическим контролем движений. Современные ортезы разрабатываются с учетом биомеханики колена и могут обеспечивать дифференцированную поддержку в различных плоскостях движения, имитируя функцию ПКС [7, 8]. Важно отметить, что применение ортезов тщательно дозируется для предотвращения избыточной зависимости и атрофии мышц.
Для наглядного сравнения хирургических и консервативных методов лечения ТКС предлагается следующая табл. 1.
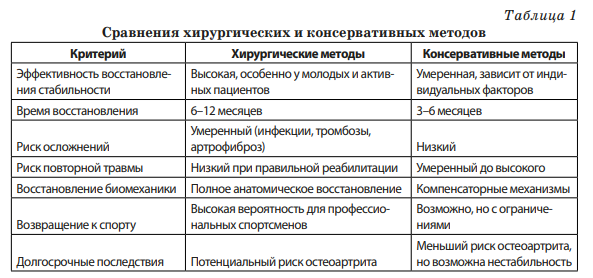
Анализируя эффективность обоих методов, следует отметить, что хирургическое лечение обеспечивает более высокую степень стабильности коленного сустава, особенно у молодых и физически активных пациентов. Это особенно важно для тех, кто планирует вернуться к занятиям спортом на высоком уровне. Консервативное лечение может быть эффективным для пациентов с меньшей физической активностью или тех, кто готов модифицировать свой образ жизни.
Время восстановления при хирургическом лечении обычно длиннее и может занимать от 6 до 12 месяцев до полного возвращения к спортивной активности. Консервативное лечение позволяет вернуться к повседневной активности быстрее, обычно в течение 3–6 месяцев, однако полное функциональное восстановление может занять больше времени.
Риски, связанные с хирургическим вмешательством, включают возможность инфекции, тромбоза глубоких вен, артрофиброза и осложнений, связанных с анестезией. Консервативное лечение имеет меньший риск таких осложнений, но может быть ассоциировано с повышенным риском повторной травмы и развития нестабильности сустава в долгосрочной перспективе.
Важно отметить, что выбор между хирургическим и консервативным лечением должен основываться на индивидуальных особенностях пациента, включая возраст, уровень физической активности, наличие сопутствующих повреждений и личные предпочтения. Некоторые исследования показывают, что у определенных групп пациентов результаты консервативного лечения могут быть сопоставимы с хирургическими методами, особенно если учитывать долгосрочные последствия и качество жизни.
В контексте долгосрочных последствий, хирургическое лечение может быть ассоциировано с повышенным риском развития остеоартрита в более позднем возрасте, хотя это компенсируется лучшей стабильностью сустава. Консервативное лечение может иметь меньший риск остеоартрита, но повышенный риск хронической нестабильности колена.
Комплексная реабилитация с акцентом на функциональное восстановление
Практика лечения травм крестообразной связки (ТКС) привела к разработке нового подхода к реабилитации, интегрирующего физические, функциональные и психологические аспекты восстановления. Ключевые компоненты этого подхода включают:
1. Раннее функциональное восстановление.
2. Интеграция нейромышечной тренировки.
3. Психологическая поддержка.
4. Применение технологий биологической обратной связи.
5. Индивидуализация программы реабилитации.
6. Регулярный мониторинг прогресса.
В табл. 2 представлено сравнение традиционного и инновационного подходов к реабилитации.
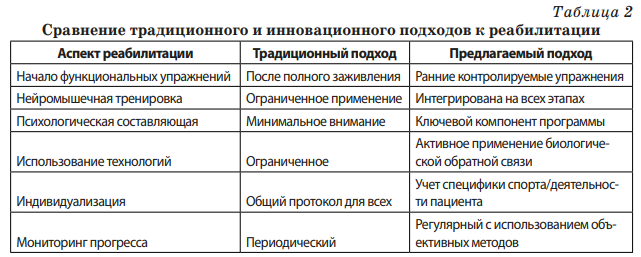
Ключевым элементом нового подхода является акцент на раннее функциональное восстановление [3–5]. Инновационная методика предполагает начало контролируемых функциональных упражнений уже в первые дни после операции или травмы. Это включает изометрические упражнения для четырехглавой мышцы бедра, ранние движения с закрытой кинетической цепью и постепенное увеличение осевой нагрузки. Ранняя активация мышц и восстановление паттернов движения способствуют улучшению проприоцепции, уменьшению отека и предотвращению мышечной атрофии. Все упражнения выполняются в безопасном диапазоне движений, не создающем чрезмерной нагрузки на восстанавливающуюся связку.
Также интеграция нейромышечной тренировки стала важным компонентом разработанной программы. Этот вид тренировки включает упражнения на баланс, координацию и контроль движений. Начиная с простых заданий на стабильной поверхности, программа прогрессирует до сложных упражнений на нестабильных платформах с добавлением когнитивных задач. Такой подход позволяет восстановить не только механическую стабильность сустава, но и его нейромышечный контроль, что критически важно для предотвращения повторных травм [1, 3].
Особое внимание в новом подходе уделяется психологическому аспекту реабилитации. Программа включает техники визуализации, работу над постановкой целей и стратегии преодоления страха повторной травмы. Пациенты учатся распознавать и контролировать свои эмоциональные реакции, связанные с процессом восстановления. Регулярные сессии с психологом, специализирующимся на спортивной реабилитации, помогают поддерживать мотивацию и психологическую устойчивость на протяжении всего процесса восстановления.
Инновационным элементом подхода стало использование технологий биологической обратной связи. Применяются специальные устройства, позволяющие пациентам в режиме реального времени отслеживать качество выполнения упражнений. Это включает системы анализа движений, платформы с сенсорами давления и электромиографические датчики. Визуальная и аудиальная обратная связь помогает пациентам лучше контролировать свои движения, способствует более эффективному восстановлению нервно-мышечных связей и повышает мотивацию к тренировкам.
Более того, индивидуализация программы реабилитации с учетом специфики вида спорта или профессиональной деятельности пациента стала ключевым аспектом нового подхода. Для спортсменов разрабатываются специфические протоколы, учитывающие биомеханические особенности их вида спорта. Например, для футболистов особое внимание уделяется упражнениям на ротационную стабильность и резкие смены направления движения, в то время как для бегунов акцент делается на плавном наращивании беговой нагрузки и работе над техникой бега.
Важным элементом нового подхода стало внедрение регулярного мониторинга прогресса пациента с использованием объективных методов оценки. Это включает периодическое проведение изокинетического тестирования для оценки силы мышц, анализ походки с использованием системы захвата движения, и функциональные тесты, имитирующие спортивные движения. Такой комплексный мониторинг позволяет не только оценивать эффективность реабилитации, но и своевременно выявлять потенциальные проблемы, что дает возможность оперативно корректировать программу восстановления.
Опыт применения данного комплексного подхода показывает, что пациенты демонстрируют более быстрое восстановление функции колена, меньше опасаются повторной травмы и быстрее возвращаются к привычному уровню активности. Особенно заметны улучшения в показателях проприоцепции и нейромышечного контроля, что критически важно для долгосрочной стабильности сустава.
ДОЛГОСРОЧНЫЕ РЕЗУЛЬТАТЫ И КАЧЕСТВО ЖИЗНИ ПАЦИЕНТОВ
Анализ долгосрочных результатов лечения травмы крестообразной связки (ТКС) и их влияния на качество жизни пациентов представляет собой критически важный аспект в оценке эффективности различных методов терапии. Этот анализ позволяет не только оценить физические параметры восстановления, но и понять, насколько успешно пациенты возвращаются к полноценной жизни и активности в долгосрочной перспективе.
Отдаленные последствия различных методов лечения ТКС могут существенно различаться. При хирургическом лечении наблюдается тенденция к лучшей стабильности коленного сустава в долгосрочной перспективе, что особенно важно для пациентов, ведущих активный образ жизни или занимающихся спортом. Однако хирургическое вмешательство также связано с повышенным риском развития остеоартрита в более позднем возрасте. Консервативное лечение, с другой стороны, может приводить к менее выраженной стабильности сустава, но потенциально меньшему риску остеоартрита.
Для наглядного представления долгосрочных результатов лечения ТКС предлагается следующая табл. 3.
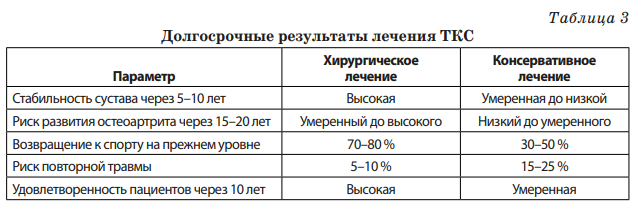
Влияние выбранного метода лечения на качество жизни пациентов является многофакторным и зависит от индивидуальных особенностей каждого случая. Пациенты, прошедшие хирургическое лечение, часто сообщают о высокой удовлетворенности результатами в долгосрочной перспективе, особенно в отношении стабильности колена и возможности возвращения к активному образу жизни. Однако некоторые пациенты отмечают периодические боли или дискомфорт, связанные с послеоперационными изменениями.
Пациенты, выбравшие консервативное лечение, могут испытывать меньше проблем, связанных с послеоперационными осложнениями, но чаще сталкиваются с чувством нестабильности колена, особенно при высоких физических нагрузках. Это может приводить к ограничению некоторых видов активности и потенциальному снижению качества жизни в долгосрочной перспективе.
Важным аспектом долгосрочных результатов является психологическое состояние пациентов. Исследования показывают, что независимо от выбранного метода лечения, пациенты могут испытывать страх повторной травмы, что влияет на их повседневную активность и качество жизни. Здесь особенно значимой становится роль психологической поддержки в процессе реабилитации.
Интеграция психологической составляющей в процесс лечения ТКС показывает многообещающие результаты в улучшении долгосрочных исходов. Пациенты, получавшие комплексную психологическую поддержку, демонстрируют:
1. Более высокий уровень удовлетворенности результатами лечения.
2. Лучшую адаптацию к возможным ограничениям физической активности.
3. Меньший уровень тревожности и страха повторной травмы.
4. Более успешное возвращение к профессиональной и спортивной деятельности.
5. Общее улучшение качества жизни и психологического благополучия.
Анализ долгосрочных результатов также выявил, что индивидуализированный подход к выбору метода лечения играет ключевую роль в достижении оптимальных результатов. Факторы, такие как возраст пациента, уровень физической активности, профессиональные требования и личные цели, должны тщательно учитываться при принятии решения о тактике лечения.
Особое внимание следует уделить вопросу возвращения к спортивной активности, так как это часто является ключевым фактором, определяющим удовлетворенность пациентов результатами лечения. Исследования показывают, что при правильно проведенной реабилитации, включающей психологическую поддержку, процент успешного возвращения к спорту увеличивается независимо от выбранного метода лечения.
В контексте долгосрочных результатов важно отметить роль продолжающегося мониторинга и поддержки пациентов. Регулярные осмотры, оценка функционального состояния колена и психологического статуса пациента позволяют своевременно выявлять и корректировать потенциальные проблемы, что способствует поддержанию высокого качества жизни в долгосрочной перспективе.
ЗАКЛЮЧЕНИЕ
Проведенный анализ современных подходов к лечению травмы крестообразной связки (ТКС) демонстрирует комплексность и многогранность данной проблемы в современной травматологии и ортопедии. Глубокое понимание анатомии и функций передней крестообразной связки, раскрытое в дополнительном разделе исследования, служит фундаментом для разработки эффективных стратегий лечения и реабилитации.
Сравнительный анализ хирургических и консервативных методов лечения ТКС показал, что оба подхода имеют свои преимущества и ограничения. Выбор оптимальной тактики лечения должен основываться на индивидуальных особенностях пациента, включая возраст, уровень физической активности, сопутствующие повреждения и личные цели.
Особое внимание в исследовании было уделено новому подходу к реабилитации, интегрирующему физические, функциональные и психологические аспекты восстановления. Раннее функциональное восстановление, нейромышечная тренировка, психологическая поддержка и использование современных технологий биологической обратной связи представляют собой ключевые компоненты этого подхода. Индивидуализация программы реабилитации и регулярный мониторинг прогресса пациента с использованием объективных методов оценки позволяют оптимизировать процесс восстановления и улучшить долгосрочные функциональные результаты.
Анализ долгосрочных результатов и качества жизни пациентов после лечения ТКС подчеркивает важность комплексного подхода, учитывающего не только физические, но и психологические аспекты восстановления. Наблюдения показывают, что успешное лечение ТКС зависит от точной диагностики, правильного выбора метода лечения, качественного выполнения хирургического вмешательства (если оно необходимо) и тщательно спланированной программы реабилитации.
КОНФЛИКТ ИНТЕРЕСОВ
Автор заявляет об отсутствии конфликта интересов при написании статьи.
CONFLICT OF INTEREST
The author declare no conflict of interest involved in preparation of the article.


