Дата поступления рукописи в редакцию: 02.11.2025 г.
Дата принятия рукописи в печать: 14.11.2025 г.
Date of receipt of manuscript at the editorial office: 11/02/2025.
Date of acceptance of the manuscript for publication: 11/14/2025.
ВВЕДЕНИЕ
Проблема бесплодия, затрагивающая значительную часть мирового населения, в своих абсолютных формах, таких как аплазия герминативных клеток, преждевременная недостаточность яичников или ятрогенные повреждения вследствие терапии рака, остается неразрешимой с использованием стандартных методов вспомогательных репродуктивных технологий (ВРТ) [1]. Технология in vitro гаметогенеза (IVG) — процесс создания функциональных гамет (сперматозоидов и яйцеклеток) из соматических клеток пациента, предварительно репрограммированных в индуцированные плюрипотентные стволовые клетки (ИПСК), который представляет собой потенциально революционный подход репродуктивной медицины [2]. Теоретически, IVG позволяет получить неограниченный источник аутологичных гамет, что открывает перспективы для пациентов, утративших герминативные клетки. Особую актуальность это направление приобретает в контексте онкофертильности, предлагая гипотетическую, хотя и отдаленную, возможность восстановления фертильности у пациентов, прошедших гонадотоксичную химио- или лучевую терапию, особенно в препубертатном периоде, когда криоконсервация зрелых гамет невозможна [3].
Несмотря на значительный оптимизм, фундаментальная научная проблема заключается в рекапитуляции in vitro всего сложнейшего процесса гаметогенеза. In vivo этот процесс охватывает десятилетия (в случае оогенеза), включает точную спецификацию примордиальных герминативных клеток (PGC), их миграцию, сложное взаимодействие с соматическими клетками гонад, прохождение мейоза и два раунда тотального эпигенетического репрограммирования [2]. Хотя в моделях грызунов были достигнуты значительные успехи, включая рождение жизнеспособного потомства из ИПСК-производных гамет, трансляция этой технологии на человека сталкивается с фундаментальными препятствиями [4]. Эти барьеры ставят под серьезное сомнение безопасность, генетическую стабильность и функциональную жизнеспособность гамет, полученных in vitro [5].
Целью настоящей работы является проведение систематического анализа современного состояния и критическая оценка клинико-биологических барьеров и перспектив создания жизнеспособных гамет человека из индуцированных плюрипотентных стволовых клеток.
Для достижения этой цели были поставлены следующие задачи:
Систематизировать и проанализировать современные протоколы реконституции женской герминативной линии in vitro, сфокусировавшись на 3D-моделях и проблеме мейотического созревания.
Систематизировать и проанализировать прорывные подходы к реконституции мужской герминативной линии, включая ксенотрансплантацию, органоидные системы и методы прямой индукции мейоза.
Идентифицировать и критически оценить ключевые биологические барьеры, препятствующие получению функциональных гамет человека, включая мейотическую остановку, генетическую нестабильность и риски эпигенетической безопасности (в частности, нарушения геномного импринтинга).
Проанализировать трансляционные перспективы IVG (клинические и исследовательские) в контексте текущего этико-правового и регуляторного ландшафта.
Научная новизна работы заключается в оригинальном авторском синтезе, который не просто суммирует последние достижения, но и фокусируется на неразрывной связи между недавними прорывами в протоколах культивирования и фундаментальными, зачастую усугубляющимися, проблемами эпигенетической безопасности. В работе проводится критическая оценка адекватности текущих критериев безопасности («золотого стандарта») и анализируется, как новейшие протоколы (например, форсированная прямая индукция мейоза) могут создавать новые, еще не изученные эпигенетические риски, отодвигая клиническое применение технологии.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Методологическая база настоящего исследования построена на принципах систематического обзора и сравнительного контент-анализа актуальной научной литературы. Для выявления общих тем, идентификации технологических прорывов, анализа существующих противоречий и определения нерешенных проблем в исследуемой области применялся качественный (нарративный) синтез данных.
Теоретической и эмпирической базой послужили научные публикации, проиндексированные в ведущих международных базах данных Scopus и Web of Science, а также данные, доступные через репозитории PubMed и MDPI. Поисковая стратегия охватывала период с 1 января 2015 г. по май 2025 г., что позволило обеспечить максимальную актуальность анализируемых данных. Поисковые запросы включали различные комбинации следующих ключевых терминов: «in vitro gametogenesis», «iPSC», «human induced pluripotent stem cells», «oogenesis», «spermatogenesis», «PGCLC», «epigenetic safety», «meiosis», «genomic imprinting», «artificial ovary», «reconstitution».
Критерии включения источников были следующими: 1) Публикации в рецензируемых научных журналах, преимущественно Q1 и Q2; 2) Период публикации; 3) Язык: английский; 4) Тематика: оригинальные исследования и обзорные статьи, посвященные протоколам дифференциации гамет человека и мыши из ИПСК, анализу безопасности (генетической и эпигенетической) и регуляторным аспектам IVG. Критериями исключения служили: 1) источники, не прошедшие рецензирование; 2) блоги, прессрелизы, новостные статьи и другие неакадемические ресурсы.
Для обработки данных применялся сравнительный анализ сопоставления эффективности, ограничений и рисков различных протоколов (например, оогенез и сперматогенез; in vivo ниша и in vitro органоид). Контент-анализ использовался для систематизации ключевых биологических и регуляторных барьеров. Авторский синтез применялся для формирования выводов о трансляционном разрыве между успехами в доклинических моделях грызунов и фундаментальными проблемами в исследованиях на клетках человека.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Реконституция женской герминативной линии: прогресс и барьеры в моделировании оогенеза
Рекапитуляция оогенеза in vitro остаётся одной из самых трудных задач регенеративной медицины: в отличие от непрерывного сперматогенеза у взрослых, женский оогенез in vivo жёстко связан с формированием фолликула — трёхмерной структуры тесного паракринного взаимодействия ооцита с клетками гранулёзы и теки [6]. Стандартные 2D-культуры не поддерживают длительный рост фолликулов, поэтому развиваются 3D-системы, или «искусственные яичники» [7]. Современные протоколы создают овариальные органоиды путём агрегации PGCLCs из ИПСК с предшественниками соматического окружения, поскольку только 3D-структура обеспечивает нужную паракринную сигнализацию для инициации и поддержания фолликулогенеза [6, 8].
Ключевое ограничение — источник соматических клеток: наиболее успешные реконструированные яичники (xrOvary) ксеногенны и используют соматические клетки из эмбрионов мыши, что, несмотря на прогрессию мейоза в человеческих PGCLCs, непригодно для клиники и осложняет интерпретацию из‑за межвидовых различий в сигналах [9]. Хотя индуцирование FOSLCs из человеческих ИПСК активно развивается, их функциональная эквивалентность и способность поддерживать полный цикл фолликулогенеза in vitro не доказаны; неспособность воссоздать аутентичную соматическую нишу остаётся основной причиной сбоев созревания ооцитов [6, 9]. Кроме того, для созревания человеческих фолликулов требуется культивирование более 120 дней, что диктует необходимость динамических перфузионных систем: статические 3D-гели не обеспечивают достаточного снабжения питательными веществами [10].
Критический барьер: асинхронность созревания и остановка мейоза
Даже в наиболее продвинутых 3D-системах ооциты, полученные из ИПСК, демонстрируют феномен остановки созревания (maturation arrest). Они либо не возобновляют мейоз, либо останавливаются на стадии Metaphase I (MI), не достигая компетентной для оплодотворения стадии Metaphase II (MII) [11]. In vivo ооцит находится в аресте профазы I десятилетиями, поддерживаемый сигналами из фолликула. In vitro, при извлечении из фолликула, происходит спонтанное возобновление мейоза, но оно часто оказывается аномальным [12].
Это приводит к фундаментальной проблеме: асинхронности между ядерным созреванием (прогрессия мейоза) и цитоплазматическим созреванием (накопление мРНК, белков и митохондрий, необходимых для раннего эмбриогенеза) [13]. Для решения этой проблемы в клинической практике in vitro созревания (IVM) были разработаны продвинутые протоколы.
Новейшим подходом, иллюстрирующим эту проблему, является двухфазная (biphasic) IVM [14]. Этот протокол разделяет процесс на два этапа. В фазе 1 (Pre-IVM) ооциты культивируются в среде, имитирующей интрафолликулярное окружение и активно подавляющей мейоз ([например, с использованием ингибиторов фосфодиэстеразы 3A (PDE3A) или аналогов C-type natriuretic peptide (CNP)]). Это дает цитоплазме дополнительное время до 24 часов догнать ядро и завершить цитоплазматическое созревание. В фазе 2 (IVM) ооциты переносятся в стандартную среду IVM для индукции финального созревания до стадии MII.
Разработка таких сложных двухфазных протоколов является, по сути, признанием неудачи в создании полноценного искусственного яичника. Исследователи вынуждены применять фармакологические костыли для имитации тех сложных паракринных сигналов, которые в норме обеспечивает фолликулярная ниша [15]. Этот подход может решить тактическую задачу (получение MII-ооцитов), но он не решает стратегическую проблему аутентичности всего процесса гаметогенеза. Это оставляет открытым главный вопрос о долгосрочной компетенции и, что важнее, эпигенетической безопасности ооцитов, подтолкнутых к созреванию химическим путем.
Реконституция мужской герминативной линии: на пути к полному сперматогенезу in vitro
В отличие от оогенеза, протоколы дифференциации ИПСК в сперматогониальные стволовые клетки (SSCs) in vitro являются относительно установленными [16]. Однако индукция полного цикла сперматогенеза, от SSC через мейоз к формированию гаплоидных сперматид, in vitro остается чрезвычайно сложной задачей [17].
Стандартным методом оценки герминативного потенциала ИПСК-производных клеток стала ксенотрансплантация. В рамках этого подхода (кейс-стади), герминативные клетки-предшественники, полученные из ИПСК человека, трансплантируются в семенные канальцы стерильных мышей-реципиентов [18]. В этой in vivo, хоть и чужеродной, нише, обеспечиваемой мышиными клетками Сертоли и Лейдига, клетки человека способны выживать, дифференцироваться, экспрессировать маркеры PGC (например, VASA) и корректно локализоваться у базальной мембраны канальцев, имитируя развитие in vivo. Этот метод успешно используется для валидации того, что клетки в принципе обладают герминативным потенциалом, и даже для изучения патогенеза бесплодия, например, у пациентов с AZF-делециями.
Однако ксенотрансплантация является методологическим черным ящиком [18]. Она подтверждает наличие потенциала, но не раскрывает механизмы, которые этот потенциал реализуют. В связи с этим, данный метод не может быть перенесен в клинику. Это доказывает, что соматическая ниша семенника предоставляет критические, но до сих пор не полностью идентифицированные факторы, которые пока невозможно адекватно воспроизвести in vitro.
Прорыв в реконституции: полный цикл in vitro и прямая индукция мейоза
Последние несколько лет ознаменовались появлением двух принципиально разных, конкурирующих подходов к преодолению барьера in vitro сперматогенеза.
Первый путем является био-реконституция. Недавние исследования сообщают о достижении полного процесса сперматогенеза in vitro с использованием 3D-систем органоидов семенника человека [19]. Утверждается, что в этих культурах, воссоздающих архитектуру семенных канальцев, наблюдаются все стадии: митотическое деление сперматогониев, мейоз сперматоцитов и спермиогенез с формированием морфологически корректных гаплоидных сперматид. Критически важным заявлением в этой работе является то, что полученные сперматиды обладают нормальным статусом метилирования импринтированных генов. Если это подтвердится, это станет огромным шагом к решению проблемы эпигенетической безопасности.
Вторым путем является молекулярная инженерия. Почти одновременно была предложена радикально иная методология: прямая индукция мейоза из ИПСК, полностью минуя стадию PGC и длительное культивирование [20]. Этот 15‑дневный протокол использует агрессивный набор из химических соединений и факторов транскрипции. Ключевые компоненты включают: 1) Ингибитор DNMT1 (для принудительного и быстрого стирания метилирования ДНК) и 2) Оверэкспрессию про-мейотических (например, HOXB5, BOLL) и антиапоптотических (BCL2) факторов. В результате, по сообщениям, клетки входят в мейоз, формируя синаптонемные комплексы и достигая стадий лептотены/зиготены.
В настоящее время наблюдается два расходящихся пути к мужскому IVG. Био-реконституция пытается медленно и точно воссоздать естественный процесс в органоиде, что теоретически обещает большую эпигенетическую безопасность за счет прохождения клетками естественных чекпоинтов [19]. Молекулярная инженерия быстра, эффективна, но несет колоссальные, неизученные эпигенетические риски [20]. Принудительное стирание метилирования с помощью ингибитора DNMT1 является грубой силой, которая может быть неполной, неточной и катастрофической для деликатных паттернов геномного импринтинга.
Визуальный синтез: протоколы, прорывы и барьеры
Для систематизации представленных данных, в табл. 1 приводится сравнительный анализ современных подходов к IVG.
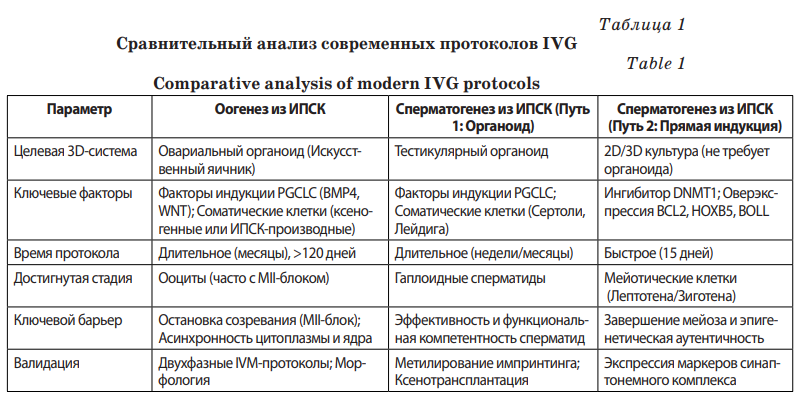
Оогенез из ИПСК в овариальном органоиде с индукцией PGCLC (BMP4, WNT) и соматической поддержкой требует длительных протоколов (>120 д) и часто завершается MII-блоком из‑за рассинхронизации цитоплазмы и ядра; валидация — двухфазный IVM и морфология. Тестикулярный органоид (путь 1) при участии соматических клеток даёт гаплоидные сперматиды за недели — месяцы, но ограничен низкой эффективностью и сомнительной функциональностью (валидация: импринтинг, ксенотрансплантация). Прямая индукция (путь 2) в 2D / 3D быстрый (~15 д), использует ингибиторы DNMT1 и оверэкспрессию BCL2/HOXB5/BOLL, приводит к мейотическим клеткам (лептотена / зиготена), но остаётся проблема завершения мейоза и эпигенетической аутентичности (валидация: маркеры синаптонемного комплекса). На рис. 1 представлена схема новейшего протокола прямой индукции мейоза.
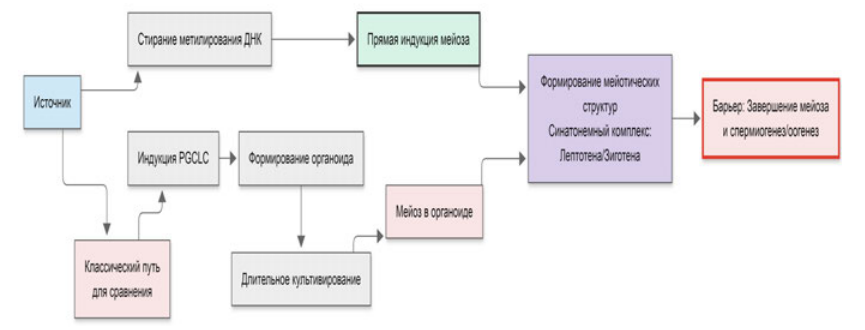
Рис. 1. Схема протокола прямой индукции мейоза из ИПСК. Fig. 1. Schematic diagram of the direct meiosis induction protocol from iPSCs.
Фундаментальные барьеры и оценка безопасности для клинической трансляции
Клиническая трансляция IVG упирается в небольшие, статистически фиксируемые риски эпигенетических изменений, унаследованные от ИПСК, прежде всего в эпигенетическую безопасность [21]. Репрограммирование соматической клетки в ИПСК и её дифференциация в гамету должны корректно повторить два крупномасштабных события: полное стирание соматической эпигенетической памяти и стирание родительского импринтинга с его восстановлением по полу гаметы.
Выделяются два основных сбоя. Первый — неполное репрограммирование: ИПСК нередко сохраняют эпигенетическую память исходных клеток, что искажает дифференцировку герминативной линии и ведёт к аберрантной экспрессии генов [22]. Второй — нарушения импринтинга: критические локусы (например, H19, IGF2) часто имеют аномальные и нестабильные паттерны метилирования в ИПСК-производных клетках, а использование гамет с такими дефектами несёт прямой риск тяжёлых нарушений развития у потомства [23, 24].
На этом фоне формируется запрос на «золотой стандарт» эпигенетической безопасности до любых клинических испытаний: мультиомное сходство с естественными гаметами (транскриптом, полным метиломом, профили гистоновых модификаций), демонстрация безопасности и фертильности на нескольких поколениях животных, а также морфологически и мультиомно нормальное развитие человеческих эмбрионов in vitro до 14 дней [25]. Возникает трансляционный парадокс: чтобы доказать безопасность IVG-гамет, нужно создавать человеческие эмбрионы и проводить их всесторонний, включая деструктивный, анализ, тогда как актуальные руководства (например, ISSCR) и законы большинства стран (например, ЕС) это запрещают, даже в исследовательских целях [26]. На рис. 2 показаны основные барьеры эпигенетической безопасности в IVG.
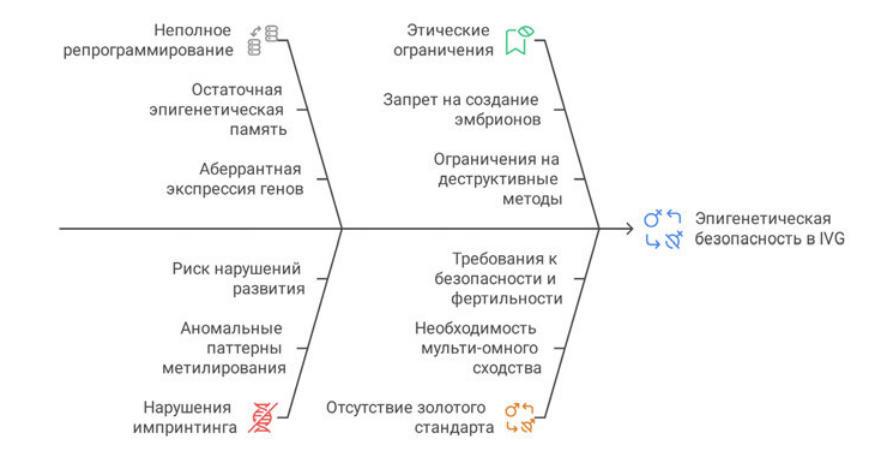
Рис. 2. Основные барьеры эпигенетической безопасности в IVG. Fig. 2. Key barriers to epigenetic safety in IVG
Таким образом, путь к необходимой валидации технологии заблокирован этическими ограничениями, которые эта же технология и порождает.
Генетическая стабильность: анеуплоидия и мутагенез
ИПСК по природе генетически нестабильны: репрограммирование может индуцировать мутации [24], а длительное культивирование, необходимое для многомесячных протоколов IVG, ведёт к селекции клеток с хромосомными аномалиями и ростовым преимуществом [27]. В линиях ИПСК и ЭСК человека регулярно выявляют рекуррентные нарушения — анеуплоидии (часто трисомии 12 и 17) [27, 28] и вариации числа копий (CNVs), которые накапливаются с временем культивирования [24].
Хотя крупные анеуплоидии теоретически могут быть отсеяны на этапе ПГТ-А, остаётся скрытая угроза: точечные мутации и CNVs в ИПСК-гаметах могут ускользать от стандартного скрининга [24, 27]. В отличие от in vivo, где действуют строгие механизмы контроля качества (например, апоптоз дефектных герминативных клеток), условия in vitro могут способствовать выживанию генетически аномальных гамет; более того, ряд новых протоколов (например, прямая индукция мейоза) сознательно используют антиапоптотические факторы (BCL2) для повышения эффективности [20]. В результате возникает риск получения гамет с de novo мутациями и их передачи потомству.
Клинико-биологические перспективы и регуляторный ландшафт
Перспективы IVG целесообразно рассматривать в двух горизонтах и для двух применений. Долгосрочная клиническая цель, лечение бесплодия, по оценке большинства экспертов остаётся делом отдалённого будущего, вероятно, на десятилетия [5]. Наиболее этически оправданный и востребованный сценарий– онкофертильность: для пациентов, особенно препубертатных, проходящих гонадотоксичную терапию, криоконсервация гонадной ткани с последующим репрограммированием соматических клеток в ИПСК может стать единственным шансом на генетически родное потомство.
Краткосрочно IVG уже служит незаменимой исследовательской платформой [29], позволяя моделировать ранний гаметогенез, миграцию PGC, молекулярные механизмы мейоза, причины генетически обусловленного бесплодия (например, остановку созревания ооцитов) и механизмы установления/стирания импринтинга. Тогда как общественная дискуссия почти полностью сосредоточена на «создании детей» [30], реальная научная ценность в ближайшие десятилетия — в использовании IVG как инструмента фундаментальной биологии [31]. Этот разрыв порождает завышенные ожидания и осложняет взвешенные этические и регуляторные дебаты.
Регуляторная среда неоднородна, фрагментирована и в целом запретительна [32]. ЕС демонстрирует наиболее строгий подход: «Закон о защите эмбрионов» в Германии прямо запрещает модификации герминативной линии, а «Конвенция Овьедо» накладывает жёсткие ограничения; возможна правовая квалификация ИПСК-гамет как ATMP с необходимостью прохождения процедур CTR.
В США действует «лакунарный» подход: прямых федеральных запретов на исследования нет, но FDA блокирует федеральное финансирование и одобрение клинических испытаний, связанных с редактированием герминативной линии или созданием эмбрионов из искусственно полученных гамет. В Японии регулирование мягче для исследований: руководства MLHW допускают редактирование герминативной линии в исследовательских целях, строго запрещая репродуктивное применение.
ЗАКЛЮЧЕНИЕ
Проведенный систематический анализ современного состояния исследований по созданию гамет из ИПСК позволяет сформулировать следующие ключевые выводы.
У грызунов IVG уже доказана (вплоть до рождения фертильного потомства, включая однополых), тогда как у человека исследования лишь переходят от стабильной индукции PGCLC к первым попыткам полного гаметогенеза in vitro — через 3D-органы или прямую индукцию мейоза. Трансляцию на человека тормозят два связных барьера: биологический — невозможность полноценно воссоздать соматическую нишу (дефекты сигнализации, асинхронность, сбои мейоза, остановка созревания), и безопасностный — высокий, плохо контролируемый риск генетической и особенно эпигенетической нестабильности, усиливаемый длительным культивированием.
Таким образом, поставленные в работе цели достигнуты. Показано, что, несмотря на медийный и общественный фокус на репродуктивном потенциале IVG, практическая значимость технологии в обозримом будущем (10–20 лет) заключается не в клиническом применении, а в ее использовании как уникальной исследовательской платформы. IVG позволяет моделировать in vitro те аспекты раннего гаметогенеза, мейоза, геномного импринтинга и патогенеза бесплодия, которые невозможно изучать на человеке in vivo. Безопасное клиническое применение, если оно когда‑либо станет возможным, потребует не только революционных технологических прорывов в культивировании, но и разработки неинвазивных методов оценки «золотого стандарта» эпигенетической безопасности и фундаментального пересмотра текущих регуляторных и этических парадигм.
КОНФЛИКТ ИНТЕРЕСОВ
Авторы заявляют об отсутствии конфликта интересов при написании статьи.
CONFLICT OF INTEREST
The authors declare no conflict of interest involved in preparation of the article.


