Вступление
Проблема рецидива болевого синдрома у пациентов с классической невралгией тройничного нерва (КНТН) после проведенного хирургического лечения представляется важной и актуальной, несмотря на успехи в диагностике заболевания и совершенствование подходов к отбору пациентов и отработанной хирургической тактики. За последние 5 лет в регистре Национальной медицинской библиотеки (Pubmed, США) индексируется 127 работ, посвященных рецидивам КНТН, что обуславливает актуальность их дальнейшего изучения.
Повторные вмешательства при рецидивах КНТН по данным различных авторов выполняются в 3–16% случаев [1, 2, 3]. Среди интраоперационных наблюдений, регистрируемых при проведении ревизионных операций, можно выделить несколько групп: недостаточно выполненная декомпрессия артерии, сохраненная на первой операции вена, смещение протектора, наличие выраженного спаечного процесса, либо отсутствие явной причины рецидива.
Тактика проведения хирургических вмешательств при рецидивах КНТН также вариативна. Некоторые авторы предпочитают выполнять ревизию корешка в ранние сроки (дни, месяцы), другие предлагают выжидательную тактику, так как известны случаи наступления отсроченного эффекта васкулярной декомпрессии на протяжение нескольких месяцев и иногда — лет. Не во всех опубликованных работах оцениваются особенности болевого синдрома (наличие нейропатического компонента), а также тип сосудистой компрессии. Настоящее исследование проведено с целью уточнения причин развития рецидивов болей в послеоперационном периоде в группе проспективно наблюдаемых пациентов.
Материалы и методы
С января 2012 года по май 2017 года в Центре по поводу классической невралгии тройничного нерва (1-го и 2-го типов) оперированы 257 пациентов (154 женщины, 103 мужчины). Медиана возраста составила 59 лет. Пациенты включены в нерандомизированную проспективную серию, оперированных по единому протоколу отбора и дооперационного обследования, хирургического пособия и послеоперационного катамнестического наблюдения. Постановка диагноза основывалась в первую очередь на особенностях клинической картины заболевания и на соответствии болевого синдрома критериям Международной классификации головной боли, ICHD–III [4]. Болевой синдром подразделялся на 1-й и 2-й типы, согласно классификации Burchiel [5]. Динамика болевого синдрома оценивалась по шкале Barrow Neurological Institute Pain Scale, BNI-PS [6].
Рецидивом считался болевой синдром, соответствующий критериям ICHD–III. В остальных случаях болевой синдром оценивался по опроснику DN-4 [7] и устанавливались признаки нейропатического характера боли. Данный алгоритм являлся «фильтром» для отбора пациентов на повторное хирургическое лечение. Пациентам с отсутствием эффекта от операции в первые 1–7 суток и неэффективности карбамазепина проводились повторные вмешательства в одну госпитализацию. Пациенты с неполным регрессом болей как правило, получали консервативную терапию в меньших по сравнению с дооперационными дозировках и подвергались хирургическому лечению лишь при увеличении интенсивности и частоты болей, при их соответствии критериям рецидива. Пациенты с преимущественно нейропатическими болями направлялись на лечение к алгологу и в группу нейромодуляции для дальнейшего лечения, повторные васкулярные декомпрессии им не проводились.
Результаты
Рецидив болей в раннем и отдаленном периодах отмечен у 33 пациентов, что составило 13 % от общего числа пациентов в исследуемой группе. Из них, оперировано 19 (58%) пациентов. Основными причинами невыполнения повторного вмешательства были: преобладание нейропатического компонента боли, низкая оценка по шкале BNI-PS (эффективность консервативной терапии), а также отказ пациента от повторного хирургического вмешательства, либо его предпочтения в проведении менее инвазивных или неинвазивных методов лечения. Более подробное распределение пациентов указано в табл. 1.
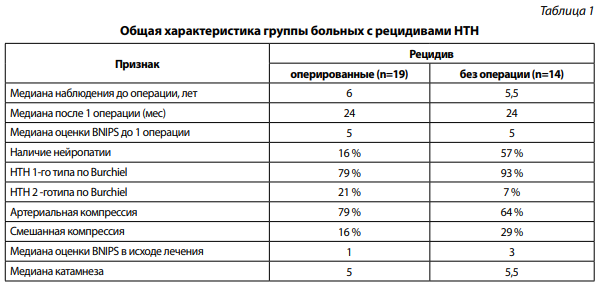
Медиана срока развития рецидивов КНТН составила 2,5 года. Важно отметить, что наиболее «поздний» срок для данного события в нашей серии составил 4 года. Этот период наблюдения у оперированных по поводу КНТН пациентов мы считаем «минимально достаточным» для формирования каких-либо заключений об эффективности проведенного лечения. Наиболее часто в нашей серии рецидивы происходили в сроке наблюдения 1 год, что наглядно иллюстрирует рис. 1, приведенный ниже.
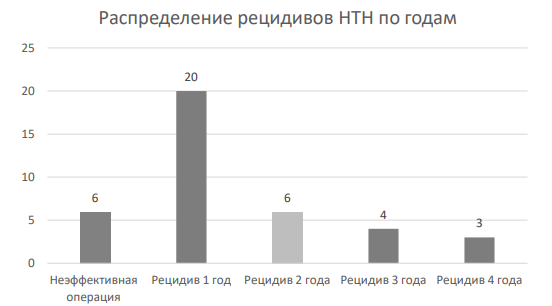
Рис. 1. Распределение пациентов с рецидивами НТН по годам наблюдения
Среди пациентов, которым не проводились повторные операции (n=14), чаще отмечались нейропатические боли. Медиана срока рецидива составила два года, при этом в данной группе отмечались наихудшие исходы (29 % пациентов периодически испытывают боли, не полностью контролируемые приемом медикаментов). Все пациенты данной группы получали консервативную терапию, наиболее частым из методов неинвазивного лечения была радиохирургия. Подробная характеристика группы изложена в табл. 2.
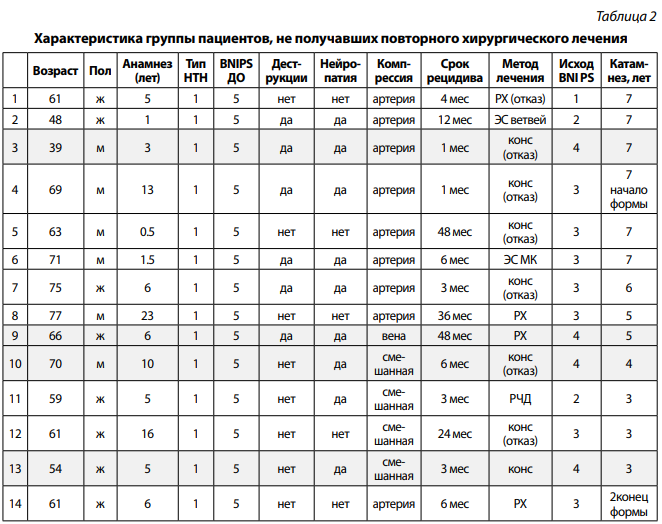
Примечание: BNIPS ДО — оценка боли до операции. Методы лечения: РХ — радиохирургическое, ЭС — электростимуляция ветвей тройничного нерва, конс — консервативное лечение, в скобках — причина, ЭС МК — электростимуляция моторной коры, РЧД — радиочастотная денервация тройничного нерва
В группе повторно оперированных пациентов медиана наблюдения перед рецидивом болевого синдрома составила два года, преобладала артериальная компрессия и в подавляющем проценте случаев болевой синдром соответствовал 1-му типу по Burchiel.
У 9 пациентов (47%) в анамнезе был один или несколько сеансов деструктивных процедур, при этом в отличие от группы не оперированных пациентов, отмечалось меньшее количество пациентов с нейропатическими болями.
В ходе изучения полученных после проведенных ревизий и повторных декомпрессий корешка тройничного нерва, выделено несколько вариантов интраоперационных находок: 1) артерия, недостаточно отделенная или оставленная рядом с нервом (n=6,32 %); 2) наличие венозной компрессии, не устранённой при первой операции (n=12,63 %), 3) миграция или диспозиция протектора (n=1,5%).
Подробная характеристика группы оперированных пациентов с рецидивами представлена в табл. 3.
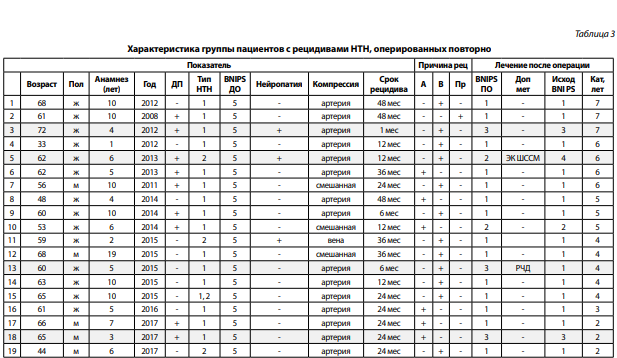
Примечание: Год — год первой операции; ДП — деструктивные процедуры; BNIPS ДО — оценка дооперационного статуса болей до 1 операции; Причины рецидива: А — артерия, В — вена, Пр — протектор; BNIPS ПО — уровень болей после второй операции; доп мет — дополнительные методы лечения: ЭК ШССМ — электростимуляция шейного сплетения спинного моза, РЧД — радиочастотная денервация тройничного нерва.
Таким образом, ведущей причиной рецидива болей была неустранённая васкулярная компрессия. Неучтенная на первой операции венозная компрессия отмечалась чаще (12 случаев против 6 с артериальной). Лишь в одном случае отмечалась миграция фрагментов фторопластового фетра, что может косвенно свидетельствовать о быстрой пролиферации арахноидальной оболочки и фиксации волокон фетра к корешку тройничного нерва.
Нам представляется важным указать несколько важных анатомических зон, которые обязательны для тщательного осмотра. В случае компрессии за счет верхней мозжечковой артерии компрессия может оказываться не только в области слияния корешка тройничного нерва и ствола мозга, но и дистально, на протяжении всей цистернальной части нерва. В области впадения корешка в Меккелеву полость в некоторых случаях петля артерии может быть скрыта костным выступом (t. suprameatalis), что может потребовать резекции костной ткани высокоскоростным бором для обеспечения адекватного осмотра. Каудальные отделы (нижняя, нижне-медиальная поверхность) тройничного нерва также нередко игнорируются при проведении декомпрессии, что может приводить к оставлению артериальных сосудов. Так, Fukushima рекомендует проводить диссекцию долек мозжечка для осмотра указанного участка нерва, указывая на необходимость предоперационного анализа МРТ в различных режимах и при совмещении изображений [8].
Венозная компрессия при КНТН, на наш взгляд, также не является казуистическим наблюдением. Принято считать, что вены небольшого размера, заключенные в арахноидальную оболочку близ корешка, можно коагулировать и пересекать безопасно. Более крупные вены, по калибру совпадающими с артериями данной области, следует сохранять и выполняя их диссекцию, отделять при помощи протектора. Важным представляется интраоперационная оценка развитости притоков верхней каменистой вены, а также дооперационное планирование с учетом данных, взвешенной по Т1 последовательности с контрастным усилением, либо магнитно резонансной ангиография.
В нашей серии единственным материалом, использованным для декомпрессии корешка, был фторопластовый фетр. По данным литературы, применение его аналога — тефлона может в ряде случаев приводить к развитию гранулем [9]. В исследуемой группе не отмечено их формирования, однако в 4 (21%) случаях при ревизии отмечено наличие выраженных сращений между арахноидальной оболочкой и оболочками нерва, усложнивших диссекцию корешка тройничного нерва. Гипотетически, наличие нескольких протекторов может провоцировать развитие рецидива болей за счет воздействия материала на корешок нерва и вызвать его компрессию; другим вариантом объяснения факта рецидива болей может быть развитие хронического воспаления в зоне операции как реакция на инородное тело. В условиях существующего арахноидита само по себе удаление протектора может не повлиять на степень регресса боли на довольно протяженное время. По этой причине, Sindou предлагает методику декомпрессии без установки протекторов на корешок [10]. Такой же тактики придерживается в своих работах Ю.А. Григорян, предлагая в качестве материала собственную мышцу пациента [11].
Заключение
У большинства оперированных по поводу КНТН пациентов отмечался полный регресс болей (85 %), они не испытывали болей и не обращались в клинику для повторного лечения, имея положительный эффект от вмешательства. У части (13%) пациентов в отдаленном периоде наблюдения отмечен рецидив болевого синдрома, из них лишь в 58 % отмечен истинный рецидив КНТН, потребовавший проведению ревизионной операции, приведшего к избавлению от болей. Эффективность повторного хирургического лечения в серии составила 79% для пациентов с полным регрессом болей. На долю пациентов, испытывающих периодические боли и контролирующих болевой синдром приемом лекарственных средств, приходится еще 16 %. У небольшого количества пациентов (2 %) васкулярная декомпрессия не привела к полному регрессу болей. Данные пациенты, страдающие помимо КНТН нейропатией тройничного нерва, представляются наиболее сложной для лечения группой. Васкулярная декомпрессия оказалась эффективной только для купирования пароксизмального компонента боли. Наличие фармакорезистентных нейропатических болей требовало проведения сеансов нейромодуляции, либо применения деструктивных процедур (радиохирургия, радиочастотная деструкция). У пациентов, получавших после васкулярной декомпрессии сеансы стимуляции ветвей тройничного нерва, регресс болей отмечался в 100% случаев. У пациентов, которым проводились деструктивные процедуры, эффективность лечения составила 78 % для группы BNI-PS 1 и 22 % для групп BNI-PS 2–3 балла, соответственно.
Таким образом, единственно эффективным методом лечения пациентов с рецидивами КНТН, у которых в структуре болевого синдрома отмечается сочетание невралгии и нейропатической боли, является мультидисциплинарный подход, подразумевающий совместное участие специалистов различных специальностей (невролог, нейрохирург, алголог, радиотерапевт).
КОНФЛИКТ ИНТЕРЕСОВ
Авторы заявляют об отсутствии конфликта интересов.
CONFLICT OF INTEREST
Тhe authors declare no conflict of interest.


