СПЛАВЫ И ИХ РАЗНОВИДНОСТИ
В машиностроении чистые металлы используются крайне редко, так как не обеспечивают необходимых эксплуатационных свойств. Широкое применение в качестве конструкционных и инструментальных материалов нашли металлические сплавы, которые по сравнению с чистыми металлами обладают более высокой прочностью и твердостью.
Сплавы — вещества, получаемые сплавлением или спеканием двух или более компонентов. Сплавы могут представлять собой системы «металл-металл» или «металл-неметалл». Например, латуни — это сплавы двух металлов — меди и цинка. Наиболее распространенные в технике материалы стали и чугуны — это сплавы железа (металл) и углерода (неметалл).
Компоненты сплава образуют однородные части сплава — фазы, имеющие при определенных внешних условиях, одинаковые состав, агрегатное состояние, кристаллическое строение (в твердом состоянии), свойства и поверхности раздела (границы), разделяющие фазы, при переходе через которые свойства резко меняются. Например, жидкий металл является однофазной системой. В процессе кристаллизации система состоит из двух фаз — жидкой и твердой. При этом свойства самих фаз существенно отличаются.
Фазы образуют структуру (строение) сплава, которая характеризуется количеством, формой, размерами и расположением фаз.
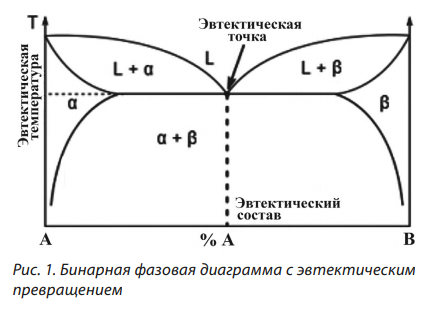
Структурные составляющие сплава как обособленные части сплава, имеющие одинаковое строение, с присущими им характерными особенностями и которые могут включать несколько фаз, например, состав, именуемый эвтектическим (рис. 1).
ТИПЫ СОЕДИНЕНИЙ, ОБРАЗУЮЩИЕ СТРУКТУРУ СПЛАВОВ
Компоненты сплава могут растворяться друг в друге, образовывать химические соединения или не вступать во взаимодействие. Соответственно с характером взаимодействия компонентов различают следующие основные типы соединений: твердые растворы, химические соединения и смеси (компоненты могут образовывать и другие типы соединений).
Твердые растворы характеризуются тем, что при их образовании один компонент (растворитель) сохраняет свою кристаллическую решетку, а другой (растворимый) отдает свои атомы в кристаллическую решетку растворителя. В результате образуется одна фаза с кристаллической решеткой компонента – растворителя. Различают твердые растворы замещения и твердые растворы внедрения (рис. 2).
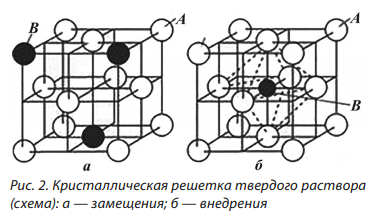
При образовании твердых растворов замещения атомы растворимого компонента В замещают атомы растворителя А в его кристаллической решетке. По взаимной растворимости компонентов различают твердые растворы замещения с неограниченной и ограниченной растворимостью компонентов. В твердых растворах с неограниченной растворимостью компонентов возможна любая концентрация растворимого компонента, вплоть до 100 %.
Условия образования твердых растворов замещения:
• компоненты принадлежат одной или смежным группам Периодической системы химических элементов и имеют близкое строение валентной оболочки электронов атомов;
• компоненты имеют кристаллические решетки одного типа;
• атомные радиусы компонентов должны иметь небольшое различие — не более 8...15 %. При большей разнице твердые растворы не образуются.
Поскольку атомные радиусы компонентов неодинаковы, при образовании твердых растворов замещения происходит искажение кристаллической решетки (рис. 3).
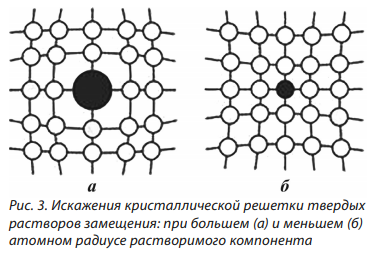
При образовании твердых растворов внедрения атомы растворимого компонента В размещаются в кристаллической решетке компонента растворителя А между его атомами. Твердые растворы внедрения образуются, если различие атомных радиусов растворителя и растворимого компонента отличаются значительно: r ≤ 0,67, где r и R — атомные радиусы растворимого компонента и растворителя соответственно.
Твердые растворы внедрения возникают между металлами и неметаллами — элементами I и II периодов Периодической системы, имеющими малые атомные размеры (Η, N, С, В), и обозначают буквами греческого алфавита: а, β, γ и т. д. или А(В), где А — растворитель, В — растворимый компонент.
Твердые растворы представляют собой одну фазу, их свойства наиболее близки свойствам металла-растворителя. Как правило, твердые растворы пластичны, хорошо деформируются в холодном и горячем состояниях. Расположение атомов компонентов в кристаллической решетке твердого раствора не упорядочено.
Для химических соединений характерно:
• что вещества, образующие химические соединения, имеют большие отличия в строении атомов и кристаллических решеток;
• кристаллическая решетка химического соединения отличается от кристаллических решеток образующих его компонентов;
• свойства химического соединения резко отличаются от свойств компонентов, которые его образовали;
• атомы в кристаллической решетке химического соединения расположены упорядоченно, т. е. атомы каждого компонента расположены закономерно и по определенным узлам кристаллической решетки;
• состав химического соединения можно описать стехиометрической формулой АтВп, где тип соединения определяется простыми целыми числами;
• химические соединения однофазны.
Соединения типа «металл-металл» (например, СuАl2) называются интерметаллидами. Интерметаллиды характеризуются металлическим типом связи. В узлах кристаллической решетки таких соединений располагаются положительно заряженные ионы, удерживаемые электронным газом.
Химические соединения типа «металл-неметалл» (например, VC, Al2O3) имеют ионный тип связи. Эта сильная связь, которая обусловливает высокую твердость и хрупкость химических соединений типа «металл-неметалл».
Смеси образуют компоненты, которые не растворяются друг в друге в твердом состоянии и не способны к химическому взаимодействию с образованием химического соединения. В сплавах типа «смесь» каждый компонент сохраняет свою кристаллическую решетку. Структура смеси гетерогенная (неоднородная), состоит из нескольких фаз. Смеси могут образовываться как компонентами, так и более сложными фазами. Например, твердыми растворами или твердым раствором и химическим соединением.
ПРАВИЛО ФАЗ
Состояние сплава зависит от внешних условий (температуры, давления) и характеризуется числом и химическим составом образовавшихся фаз. Условия существования устойчивых (равновесных) фаз описываются законом Гиббса («правилом фаз»), который устанавливает зависимость между степенью свободы системы (С), с одной стороны, и количеством фаз (Ф), находящихся в равновесном состоянии, а также компонентов (К) — с другой. Число степеней свободы системы — это число внешних и внутренних факторов (температура, давление и концентрация), которое можно изменять без изменения числа фаз. В соответствии с правилом фаз: С = К + 2 – Ф, где 2 — это количество внешних факторов — температуры и давления.
Если принять, что все превращения в металле происходят при постоянном давлении, приведенное уравнение принимает следующий вид: С = К + 1 – Ф.
Поскольку С не может быть отрицательным или дробным числом, то К + 1 – Ф > 0, т. е. число фаз, находящихся в равновесии, не может превышать число компонентов системы более чем на 1. Поэтому в 2-компонентных сплавах в равновесии может находиться не более 3-х фаз.
В качестве примера определим, как меняется число степеней свободы однокомпонентной системы (чистый металл). В жидком или твердом состоянии в такой системе имеется только одна фаза: С = 1 + 1 – 1 = 1, т. е. возможно изменение температуры без изменения фазового состава. В процессе кристаллизации или плавления в системе имеются 2 фазы — жидкая и твердая, тогда: С = 1 + 1 – 2 = 0, т. е. кристаллизация и плавление происходят при постоянной температуре, и эта температура не может быть изменена до тех пор, пока вещество не станет однофазным — твердым при кристаллизации или жидким при плавлении.
СОСТОЯНИЯ СПЛАВОВ ДВУХКОМПОНЕНТНЫХ СИСТЕМ. ПРИНЦИПЫ ПОСТРОЕНИЯ ДИАГРАММ СОСТОЯНИЯ
Диаграммы состояния сплавов двухкомпонентных систем представляют собой графическое изображение фазового состояния сплавов данной системы в зависимости от температуры и концентрации компонентов (химического состава сплава).
Диаграммы состояния играют важную роль в теории и практике материаловедения. С их помощью можно исследовать фазовые и структурные превращения сплавов. Анализ диаграмм дает возможность предвидеть изменение свойств сплавов и назначать оптимальные режимы термической обработки.
Диаграммы строятся для равновесного состояния сплавов, которое соответствует минимальному значению свободной энергии системы. Такое состояние достигается при малых скоростях охлаждения или нагрева.
При построении диаграмм температуру откладывают по оси ординат, концентрацию компонентов — по оси абсцисс. Слева направо увеличивается количество компонента В, справа налево — компонента А. Таким образом, в начале координат находится чистый компонент А (значение по абсциссе равно нулю — содержание компонента В = 0 %); при значении абсциссы, равном 100 %, имеем чистый компонент В (рис. 4).
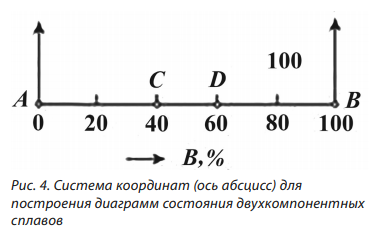
Общее содержание компонентов в сплаве равно 100 %, каждая точка на оси абсцисс соответствует определенному содержанию обоих компонентов. Например, точка С характеризует сплав, в котором содержится 40 % компонента В и 60 % компонента А, а точка D — сплав, в котором 60 % компонента В и 40 % компонента А.
Для построения диаграмм состояния сплавов используют данные, полученные с помощью кривых охлаждения, построенных для серии сплавов, состоящих из одних и тех же компонентов, но имеющих неодинаковый химический состав.
Для построения диаграмм состояния сплавов используют метод термического анализа. Он заключается в экспериментальном построении кривых охлаждения сплавов известного состава, с помощью которых определяют критические точки сплава. Кривую охлаждения строят в координатах «температура (t) – время (τ)», снимая через равные промежутки времени значения температуры. При этом охлаждение сплава должно быть медленным, что обеспечивает его равновесное состояние при всех температурах.
Критические точки сплава — это, как известно, температуры, при которых происходят структурные превращения в сплавах. На кривых охлаждения сплавов они выявляются в виде перегибов или площадок, свидетельствующих об изменении темпов охлаждения, что связано с выделением скрытой теплоты кристаллизации.
Простейшие диаграммы состояния 2-компонентных систем можно разделить на 3 основных типа:
• диаграммы состояния сплавов, компоненты которых в твердом состоянии образуют смеси;
• твердые растворы;
• химические соединения.
Диаграммы состояния ряда сплавов могут содержать элементы простейших диаграмм состояния. Это могут быть, например, диаграммы с частичной растворимостью компонентов.
При определенных (вполне конкретных) концентрациях компонентов образуются так называемые твердые растворы, при прочих концентрациях — смеси этих твердых растворов.
Диаграммы состояния сплавов, их анализ и структурные особенности будут рассмотрены и изложены далее, в продолжении.
(Продолжение следует)
ПРОМЫШЛЕННАЯ МОЗАИКА
Корпорацией «МиГ» сформирован портфель заказов до 2025 года
На конец I полугодия с. г. «Российской самолетостроительной корпорацией (РСК) “МиГ”» сформирован портфель заказов на период до 2025 г. Таким образом производственные мощности корпорации на весь этот период полностью загружены. Об этом заявил генеральный директор корпорации Илья Сергеевич Тарасенко в своем интервью газете «Коммерсантъ». 2016 г. корпорацией был завершен с выручкой на уровне 56,7 млрд руб. и чистой прибылью 5,6 млрд руб.
По словам Тарасенко И.С., поставки по оборонным заказам в 2016 г. корпорацией были полностью выполнены, а существующие проекты ведутся с учетом того, что деятельность корпорации должна быть не только полностью окупаемой, но и прибыльной. В 2017 г. корпорация рассчитывает увеличить выручку примерно на 15–17 %.
Источник: интернет-ресурс http://promvest.info/ru


