Лимфопролиферативные заболевания — группа заболеваний, морфологическим субстратом которых являются клетки лимфоидной природы.
Среди лимфопролиферативных заболеваний выделяют лимфоидные формы лейкозов — острый лимфобластный лейкоз, хронический лимфолейкоз, парапротеинемические гемобластозы и так называемые нелейкемические лимфоидные гемобластозы, включающие неходжкинские лимфомы, при которых первичный очаг поражения развивается преимущественно вне костного мозга.
Код МКБ-10: С91.1.
Диагноз пациента с лимфопролиферативным заболеванием (ЛПЗ) при первичном обследовании должен состоять из трех неотъемлемых частей:
1. Диагноз опухоли, сформулированный в соответствии с действующей классификацией Всемирной организации здравоохранения (ВОЗ).
2. Распространенность процесса — стадия (установленная в соответствии с принятыми классификационными системами).
3. Общее состояние больного (оцененное по международным критериям).
ДИАГНОЗ ОПУХОЛИ
До биопсии лимфатического узла (ЛУ) необходимо сделать общий анализ крови с подсчетом лейкоцитарной формулы, чтобы исключить необходимость выполнения биопсии у больных хроническим лимфолейкозом (ХЛЛ), острыми лейкозами или при лимфоцитозе инфекционной этиологии (инфекционный мононуклеоз, коклюш и др.).
Диагноз опухоли устанавливают на основании морфологического исследования биопсийного или операционного материала. Морфологическое исследование проводится с помощью цитологических, гистологических и иммуногистохимических методов.
Отдельные случаи нуждаются в проведении молекулярно-биологических и генетических тестов. Цитологическое исследование пунктатов, или мазков-отпечатков ЛУ, или других опухолевых очагов не является достаточным основанием для нозологической верификации лимфом.
При первичном обследовании пациента во всех случаях проводится гистологическое и иммуногистохимическое исследование инцизионной или эксцизионной биопсии патологического очага или операционного материала.
Пунктировать ЛУ для аспирации клеточной взвеси не следует. В исключительных случаях (локализация опухоли в труднодоступных анатомических зонах) объектом исследования может быть тканевой материал, полученный с помощью пистолетной («кор»-) биопсии.
Объем иммуногистохимического исследования определяет врач-патологоанатом при гистологическом изучении материала.
Протокол морфологического исследования должен содержать следующее.
1. Макроскопическое описание материала, присланного для исследования; при исследовании готовых блоков и микропрепаратов в протоколе должны быть указаны количество и идентификационные номера всех изучаемых объектов.
2. Гистологическое описание лимфомы с указанием типа роста (диффузный, нодулярный, фолликулярный и т. п.), характеристики клеточного состава (мелкие, крупные клетки, полиморфный состав, анапластическая, бластная морфология, наличие многоядерных форм, характеристика ядер), наличия реактивных и резидуальных компонентов.
3. Результаты иммуногистохимического исследования с указанием использованных антител, их клоно и подробностей окрашивания, указывающих на специфический характер реакции (например, окрашивание ядер в реакциях на TdT, bcl-6, cyclin D1; цитоплазмы в реакциях на CD79a, цитотоксические молекулы; цитоплазмы или мембраны — в реакциях нCD3, цепи иммуноглобулинов [Ig]; мембраны — в реакциях на CD20, CD10 и т. д.). Представление результатов иммуногистохимических тестов только в вид крестов (плюсов) и перечня антител недопустимо.
4. Диагностическое заключение, сформулированное в соответствии с действующей классификацией ВОЗ. Обязательным компонентом определения распространенности опухолевого процесса (стадии) является гистологическое исследование трепанобиоптата костного мозга. В процессе первичного обследования рекомендуется выполнять биопсию билатерально.
Морфологическое исследование пунктата костного мозга (стернального или другого) не заменяет гистологическое исследование трепанобиоптата.
При наличии в общем анализе крови или миелограмме лимфоцитоза, независимо от числа лейкоцитов, а также при преобладании лимфоидных клеточных элементов, атипичных лимфоцитов или подозрительных на бластные клетки в плевральной, асцитической или других биологических жидкостях необходимо выполнение иммунофенотипирования методом проточной цитометрии. Проточная цитометрия позволяет быстро провести дифференциальную диагностику опухолевого и реактивного лимфоцитоза, что важно для определения дальнейшей тактики обследования пациента. Материалом для анализа методом проточной цитофлюориметрии могут служить клетки крови, костного мозга, выпотных жидкостей, бронхоальвеолярного смыва, ликвора, гомогенизированные образцы тканей (селезенка, ЛУ и т. д.), клеточная суспензия, полученная при аспирационной тонкоигольной пункции ЛУ.
При определении стадии опухолевого процесса может потребоваться биопсия других очагов поражения, если нельзя исключить их опухолевую природу другими способами.
При рецидиве или прогрессировании заболевания обязательно выполнение повторной биопсии и морфологического исследования пораженных ЛУ или очагов, расположенных экстранодально.
Также повторная биопсия показана при наличии резидуальных очагов для подтверждения ремиссии.
Повторно аспирация и трепанобиопсия костного мозга выполняются для плановой оценки результатов лечения и при появлении клинически немотивированных цитопении и лихорадки.
Аспират костного мозга может быть информативен для оценки регенерации и диспластических изменений гемопоэза. У больных с поражением костного мозга цитологическое исследование пунктата для оценки изменений объема опухолевой инфильтрации не всегда информативно. Если у пациента с исходным поражением костного мозга при повторной биопсии не обнаружены ни опухолевая инфильтрация, ни изменения «архитектуры» костного мозга, это означает, что повторный биоптат был взят из зоны вне поражения и необходима еще одна биопсия.
РАСПРОСТРАНЕННОСТЬ ПРОЦЕССА
Определение стадии у больных лимфомами (за исключением указанных особо) осуществляется на основании классификации Ann Arbor в модификации Cotswold (табл. 1).
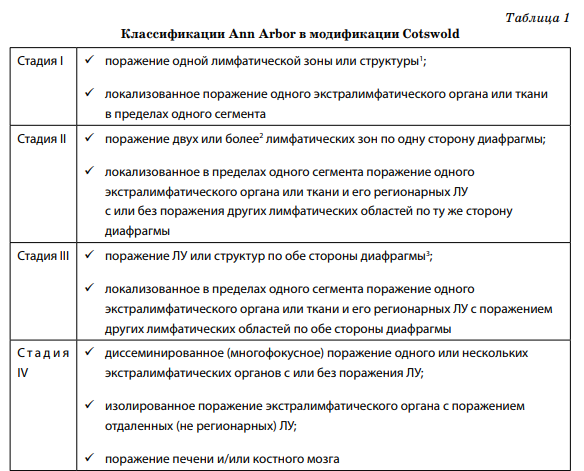
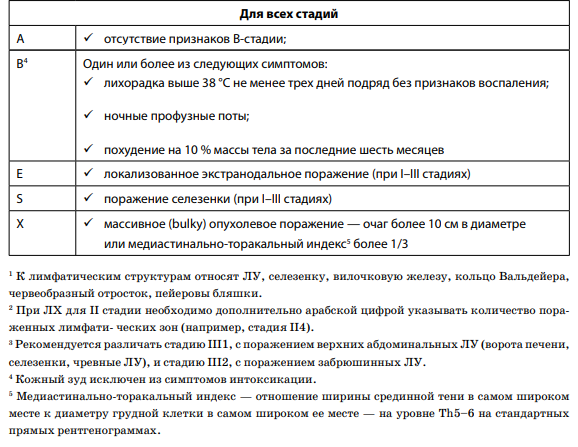
ФОРМУЛИРОВАНИЕ ДИАГНОЗА
– При формулировании диагноза необходимо указать:
– название болезни в соответствии с морфологической классификацией ВОЗ 2008 г., вариант заболевания при его наличии (морфологический или цитологический вариант, тип и т. д.; указание на редко диагностируемые первичные экстранодальные варианты, нетипичные иммунофенотипические и молекулярные варианты, обусловливающие изменение терапевтической стратегии, также могут быть включены в диагноз);
– стадию заболевания с учетом В-симптомов и других факторов риска, с указанием всех зон поражения. При поражении парных органов указывается, какой из них поражен;
– группу риска и/или прогностическую группу с указанием используемого прогностического индекса (IPI, FLIPI и т. д. — см. разделы, посвященные соответствующему заболеванию);
– осложнения, обусловленные заболеванием.
ПЛАН ОБСЛЕДОВАНИЯ БОЛЬНОГО
Клиническое обследование:
- сбор анамнеза (в том числе семейного);
– физикальный осмотр, в том числе пальпация всех доступных пальпации групп периферических ЛУ, печени, селезенки, осмотр миндалин и полости рта;
– определение наличия В-симптомов;
– определение статуса по ECOG:
0. Полностью активен, способен переносить нагрузки в том же объеме, что и до начала заболевания.
1. Ограничен в выполнении интенсивных физических нагрузок, но свободно передвигается и может выполнять легкую или сидячую работу — легкую работу по дому, работу в офисе.
2. Свободно передвигается и в состоянии себя обслуживать, но не может выполнять какую-либо работу. Проводит в постели меньше 1/2 светлого времени суток.
3. Возможность себя обслуживать ограничена. Проводит в постели большую часть светлого времени суток.
4. Не в состоянии себя обслуживать. Прикован к постели или креслу.
Лабораторные методы исследования:
– развернутый клинический анализ крови с подсчетом лейкоцитарной формулы и количества ретикулоцитов;
– общий анализ мочи;
– биохимический анализ крови (лактатдегидрогеназа [ЛДГ], мочевая кислота, мочевина, креатинин, общий белок, альбумин, билирубин, аспартатаминотрансфераза [АСТ], аланинаминотрансфераза [АЛТ], щелочная фосфатаза [ЩФ], электролиты, кальций);
– коагулограмма;
– электрофорез белков сыворотки крови;
– определение группы крови, резус-фактора;
– определение маркеров вирусных гепатитов В и С, ВИЧ;
– у женщин детородного возраста — тест на беременность.
Методы лучевой диагностики:
– рентгенография органов грудной клетки (при невозможности выполнения компьютерной томографии [КТ] в двух проекциях);
– КТ шеи, грудной клетки, органов брюшной полости и малого таза;
– ультразвуковое исследование (УЗИ) периферических, внутрибрюшных и забрюшинных ЛУ и органов брюшной полости может использоваться для контроля за лечением, но не является стандартом при установлении стадии заболевания и при оценке эффективности лечения.
Цитологическое и гистологическое исследование костного мозга.
Электрокардиограмма (ЭКГ) и эхокардиограмма (ЭхоКГ).
Эндоскопическое исследование желудка.
При наличии показаний также могут выполняться следующие методы.
Лабораторные методы исследования:
– исследование b2-микроглобулина;
– прямая проба Кумбса.
Методы лучевой диагностики:
– рентгенография костей скелета, сцинтиграфия костей скелета;
– КТ или магнитно-резонансная томография (МРТ) головного мозга;
– позитронно-эмиссионная томография (ПЭТ).
Поскольку химиотерапия (ХТ) и облучение области таза могут привести к необратимой стерильности пациента, со всеми больными детородного возраста обоих полов целесообразно обсуждать вопрос о возможности криоконсервации спермы или ткани яичника перед началом терапии.
С женщинами детородного возраста следует обсуждать вопрос о необходимости гормональной защиты от беременности, а также о методах возможной гормональной защиты яичников при проведении интенсивных программ лечения.
ОПРЕДЕЛЕНИЕ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ
Оценку эффективности лечения следует проводить в середине (после 2–3-го цикла ХТ) и после индукционного курса лечения, а также после завершения всей программы лечения (химио- или химиолучевой терапии, поддерживающей терапии и т. д.). Обследование пациента должно обязательно включать тщательный осмотр, клинические анализы, полное исследование методами лучевой диагностики, применявшимися до начала лечения.
Полная ремиссия (ПР):
1. Полное исчезновение всех проявлений заболевания, в том числе выявляемых при помощи лабораторных и лучевых методов диагностики, а также клинических симптомов, если они имели место до начала лечения.
2. Размеры ЛУ:
а) ≤ 1,5 см по наибольшему диаметру, если до начала лечения размеры ЛУ были больше 1,5 см;
б) ≤ 1,0 см по наибольшему диаметру, если до начала лечения размеры ЛУ были 1,5–1,1 см.
3. Печень, селезенка, если были увеличены до начала лечения, не пальпируются, по данным лучевых методов объемные образования в них не выявляются.
4. Костный мозг без признаков опухолевого поражения. Если результат морфологического исследования костного мозга неоднозначный, наличие или отсутствие поражения должно определяться иммуногистохимически.
Полная ремиссия считается подтвержденной, если достигнутый эффект сохраняется не менее двух недель или констатируется дальнейшее улучшение.
Неуверенная полная ремиссия (ПРн):
1. Остаточные изменения, выявляемые только при помощи лучевых методов исследования (особенно это касается остаточных объемных образований в месте массивного опухолевого поражения, чаще всего в средостении), в случае сокращения опухоли более чем на 75 % от исходных размеров по сумме двух наибольших ее диаметров. Эти остаточные изменения не должны увеличиваться в течение более чем трех месяцев.
2. По другим показателям — соответствие критериям ПР.
Частичная ремиссия (ЧР):
1. Уменьшение суммы диаметров всех измеряемых очагов (ЛУ и/или очагов экстранодального поражения) не менее чем на 50 %. Если размеры пораженных очагов менее 3 см по наибольшему диаметру, то два наибольших очага должны уменьшиться не менее, чем на 50 % по наибольшему диаметру. При наличии более чем шести очагов поражения более 3 см достаточна оценка шести наибольших очагов, доступных четкому измерению в двух перпендикулярных направлениях. При наличии медиастинальных и/или ретроперитонеальных очагов поражения они обязательно должны учитываться при измерении.
2. Отсутствие новых очагов поражения, отсутствие признаков увеличения какого-либо из ранее диагностированных очагов поражения.
3. В случае исходного поражения костного мозга статус костного мозга для определения ЧР незначим. Однако при сохранении поражения костного мозга в процессе и/или после завершения лечения обязательно уточнение характеристики опухолевых клеток.
Больные с исходным поражением костного мозга, у которых после завершения лечения клинически диагностируется ПР, но при этом сохраняется поражение костного мозга или костный мозг не может быть оценен, относятся к ЧР.
Стабилизация (Ст)
Показатели опухоли не соответствуют ни критериям ПР или ЧР, ни критериям прогрессирования.
Рецидив (после ПР) или прогрессирование (после ЧР или Ст):
1. Появление новых очагов (увеличение ЛУ или объемных образований экстранодальных локализаций) более 1,5 см в наибольшем измерении в процессе или после завершения лечения, вне зависимости от изменения размеров других очагов поражения.
2. Увеличение как минимум одного уже известного очага более чем на 25 % от минимального. Для очагов менее 1 см в наибольшем измерении — увеличение до 1,5 см и более.


