По данным Всемирной организации здравоохранения (ВОЗ, World Health Organization, WHO), грипп и ОРВИ (острые респираторные вирусные инфекции) занимают лидирующие места по частоте причин заболеваемости и смертности среди всех инфекционных заболеваний [1]. На самом деле частота ОРВИ превышает данные официальной статистики, поскольку реальное количество заболевших, не обратившихся за медицинской помощью, превышает показатели в несколько раз. По данным отчетов Федерального государственного учреждения здравоохранения «Федеральный центр гигиены и эпидемиологии Роспотребнадзора РФ» (http://www.fcgsen.ru), для некоторых категорий (дети, пожилые люди) заболеваемость ОРВИ является традиционно более высокой, чем в общей популяции [2]. Одной из задач Всемирной организации здравоохранения (ВОЗ) по борьбе с гриппом и респираторными вирусными инфекциями является разработка как вакцин, так и препаратов с противовирусным действием [3].
Этиологическую структуру ОРВИ составляют, по разным оценкам, от 300 до 320 возбудителей вирусной и бактериальной природы, среди которых имеются как известные, сохраняющие свою актуальность вирусы, так и новые высокопатогенные штаммы [4]. В отличие от вируса гриппа, они не имеют четко прослеживаемой сезонности, формируя круглогодичный пул заболеваемости органов дыхательной системы во всем мире [5]. Высокая антигенная лабильность возбудителей приводит к развитию пандемий, кроме того, периодически на эпидемической арене появляются разновидности вирусов, казалось бы, известных, но человеческий организм оказывается беззащитным против агрессии подобного возбудителя.
Для большинства этиологических агентов ОРВИ характерны пневмотропность, способность передаваться как воздушно-капельным путем, так и контактно-бытовым, фекальнооральным способами передачи [6]. Для всех ОРВИ клинически характерно сочетание общеинфекционного синдрома (лихорадка, головная боль, слабость, миалгия) с признаками поражения дыхательных путей [7]. Цитопатическое действие респираторных вирусов в отношении клеток эпителия дыхательных путей выражено на фоне иммунодефицитных состояний. Развитие, течение и неблагоприятный исход ОРВИ являются следствием некомпетентности системных и локальных иммунных факторов. Возникающие при этом взаимосвязанные нарушения способствуют рецидивирующему течению, не исключая возможности хронизации или персистенции патогенов, вызвавших заболевание [8–10].
Большинство исследователей склоняется к тому, что при ОРВИ имеют место комбинированные поражения звеньев системной антимикробной защиты. К механизмам естественной резистентности и противовирусной защиты относятся целостность эпителия слизистых оболочек дыхательных путей, система интерферонов, включающих ранние I типа — ИФН-альфа [лейкоцитарный — продуцируется лейкоцитами и другими клетками врожденного иммунитета, ИФН-бета — продуцируется фибробластами, поздние ИФН II типа (ИФН-гамма), ИФН III типа ИФНγ1, ИФНγ2 , ИФНγ3 (IL-28A, IL-28B, IL-29)] [11].
Поскольку этиотропная и патогенетическая терапия при гриппе и ОРВИ в большинстве случаев носит неотложный характер, то использование препаратов с доказанной эффективностью для практического врача является приоритетной задачей.
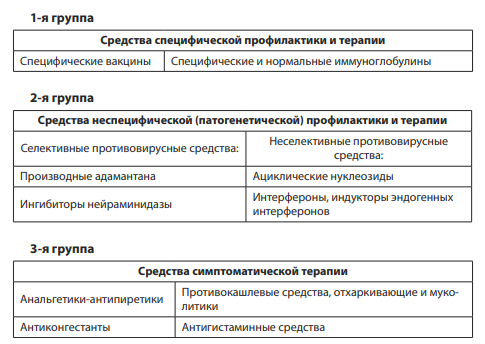
Лекарственные средства, используемые в терапии ОРВИ, можно условно разделить на три основные группы [12] (представлены ниже).
Появление в арсенале врачей нового противовирусного препарата Нобазит® (энисамия йодид, N-метил4-бензилкарбамидопиридиния йодид), производного изоникотиновой кислоты, является важным этапом борьбы с ОРВИ [13–15]. Механизм Нобазит® (энисамия йодид) основан на влиянии на структуру и процессы связывания рецепторов гемагглютинина респираторных вирусов, включая вирус гриппа. Данный механизм не дает возможности вирионам адсорбироваться к клеткам-мишеням [16]. Наличие у препарата Нобазит® интерфероногенных свойств в отношении продукции эндогенных ИНФ-α и ИНФ-γ в плазме крови делаеет его незаменимым в профилактике вирусных инфекций [17].
Ранее проведенные исследования свидетельствуют о противовоспалительных, жаропонижающих, анальгезирующих эффектах энисамия йодида, что позволяет снизить риск полипрагмазии и развития побочных реакций соответственно [18]. Анализ побочных эффектов препарата не выявил патологических изменений в составе периферической крови.
Противовирусное действие Нобазита® (энисамия йодид) продемонстрировано на Третьем противовирусном конгрессе в Амстердаме 12–14 октября 2014 г., представлены данные о снижении титра вирусной нагрузки в исследованиях in vivo и эффективность против вирусов, резистентных к осельтамивиру [19].
Цель — оценка эффективности применения в амбулаторной практике противовирусного препарата энисамия йодида в комплексной терапии острых респираторных вирусных инфекций.
МАТЕРИАЛЫ И МЕТОДЫ
В проспективное рандомизированное исследование включены 64 пациента (30 мужчин и 34 женщины) с давностью заболевания не более двух суток, не получавших предшествующей терапии противовирусными препаратами. Период проведения исследования с сентября 2019 г. по январь 2020 г. От всех больных получено письменное информированное согласие на участие в исследовании в соответствии с основами законодательства РФ «Об охране здоровья граждан, правил проведения клинической практики в РФ» (приказ МЗ РФ от 19.07.2003 № 266; приказ Рос здравнадзора от 17.10.2006 № 2325-Пр/06). Пациенты были обследованы на наличие вирусов гриппа А и B, респираторносинцитиального вируса, вируса парагриппа, корона-, рино-, аденовирусов в мазках из носоглотки методом полимеразной цепной реакции. Изучение пациентов, включенных в исследование, проведено в ООО «Лаборатория «Гемотест» (сертификат соответствия ГОСТ Р ИСО 15189–2015 (ISO 15189:2012) в области клинической лабораторной диагностики, исследований в области бактериологии, вирусологии, патологической анатомии).
Пациенты первой группы (n = 32) получали энисамия йодид в комплексе с симптоматической терапией, на курс лечения 30 таблеток (по 2 таблетки 3 раза в день в течение пяти дней непрерывно), пациенты второй группы (n = 32) получали только симптоматическую терапию: режим, диета, поливитамины, антиконгестанты, анальгетики-антипиретики, противокашлевые и отхаркивающие средства.
Клиническую эффективность проведенного лечения оценивали ежедневно в течение пяти дней и через 10 дней после терапии. Оценка была проведена по шкале Total Symptom Score — TSS, выраженности проявлений ОРВИ со 2-го по 5-й день по критериям эффективности: продолжительность заболевания; степень выраженности лихорадки; продолжительность основных клинических симптомов заболевания; относительное содержание больных, у которых зарегистрировано развитие осложнений, требующих применения антибактериальной терапии или высокотехнологичной помощи; динамика показателей иммунного и интерферонового статуса. Для проведения статистического анализа клинических признаков применялся метод сравнения количественных показателей в двух независимых группах с учетом шкалы выраженности TSS.
Для исключения бактериальной инфекции проведено микробиологическое исследование отделяемого небной, глоточной миндалины и носоглотки. В качестве дифференциально-диагностических сред для стафилококков и коринебактерий был использован кровяной солевой агар. Диагностическим считался титр 103 КОЕ/мл и выше. Выявление наличия пиогенных стрептококков проводилось с использованием экспресс-тестсистем Streptotest в день обращения пациентов. Пиогенный стрептококк выявлен до начала исследования у трех пациентов, которые были исключены из групп 1 и 2.
Общее клиническое исследование крови (гемоглобин, эритроциты, лейкоциты, лейкоцитарная формула, СОЭ) было назначено и проведено участникам исследования до лечения и после окончания приема препарата Нобазит® (на 5-й день). Иммунологическую эффективность терапии оценивали путем анализа функциональной активности нейтрофильных гранулоцитов периферической крови по их способности к поглощению частиц латекса, кислородзависимому метаболизму в тесте восстановления нитросинего тетразолия (НСТ-тест), функциональному резерву на 5-й день лечения [20]. Для определения концентрации иммуноглобулинов IgA, sIgA, IgM, IgG в сыворотке периферической крови, интерферонов применяли метод иммуноферментного анализа (ИФА). С этой целью были использованы тест-системы ООО «Вектор-Бест» (Новосибирск). Субпопуляционный состав лимфоцитов периферической крови был исследован методом проточной цитофлюориметрии с использованием аппаратного комплекса Beckman Coulter (США). В процессе исследования было определено абсолютное и относительное содержание CD3+-, CD4+-, CD8+- CD16+CD19+-, HLA-DR+-клеток. Материалом для иммунологического исследования служила периферическая кровь, взятая из локтевой вены утром строго натощак, в вакуумную систему до указанной на пробирке метки. В качестве антикоагулянта использовался К2ЭДТА.
При расчете статистических значений использовали диапазон M±m. Полученные данные обрабатывали методами вариационной статистики с применением пакетов прикладных программ SPSS for Windows 13.0. Для анализа нормальности распределения данных использовали критерий Шапиро — Уилка. Для вычисления относительного вклада клинических признаков в развитие исследуемой патологии и оценки эффективности применения терапевтических мероприятий применяли χ²-квадрат, использован доверительный интервал 75 %.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Этиологическая структура ОРВИ в группах 1 и 2 была следующей: грипп А встречался у 5 человек (7,81 %); грипп В — у 1 человека (1,50); РСинфекция — у 10 (15,6); парагрипп — у 17 человек (26,98); аденовирусная инфекция — у 16 (25,00); риновирусная — у 15 (23,40 %). Эффективность терапии была оценена нами по показателям клинического выздоровления больных и нормализации лабораторных показателей. Эффективность лечения оценивалась с помощью анализа показателей контрольных исследований, которые осуществлялись на 5-й, 30-й день (1 месяц) от начала лечения. Клиническим выздоровлением считалось стойкое исчезновение всех симптомов воспалительного процесса и восстановление лабораторных показателей периферической крови. После приема препарата Нобазит® пациентам группы 1 не потребовалось дополнительного назначения жаропонижающих препаратов. Улучшение общего состояния было отмечено через 8 ч после приема препарата Нобазит®. Температура снизилась до 37,5 °С, уменьшилась интенсивность головной боли, исчезла мышечная боль, снизились боль в горле и заложенность носа, интенсивность кашля.
По результатам анализа медианы средняя оценка по шкале общей выраженности проявлений ОРВИ в основной группе составила 5,20 (3,76–5,87), в группе сравнения — 6,49 (4,22–7,15; p<0,001). Продолжительность как системных, так и локальных проявлений ОРВИ была достоверно меньше в первой группе (р = 0,001 и р = 0,021 соответственно). Сроки купирования головной боли не имели достоверных отличий в первой и второй группах, пациенты которых получали энисамия йодид и энисамия йодид и патогенетическую терапию. Назначение дополнительной терапии потребовалось 1 (3,13 %) пациенту первой группы (принимающей энисамия йодид) по сравнению с 5 (15,60 %) пациентами из контрольной группы.
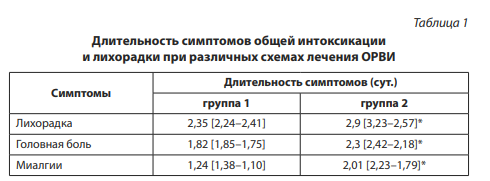
Примечание: * приведены достоверные различия между группами 1, 2, р < 0,05.
Необходимо отметить, что все пациенты, получавшие препарат Нобазит®, отметили его хорошую переносимость. Оценку лечению «отлично» и «очень хорошо» дали 32 (100 %) пациента группы 1, в то время как во второй группе аналогичные оценки поставили только 20 (58,8 %) больных. На 5-й день терапии в первой группе пациентов элиминация вируса была достигнута в 90,5 % случаев; во второй группе — в 59,4 % случаев. При оценке выраженности клинических проявлений ОРВИ по анализу отмечено снижение баллов по шкале ВАШ на 24, 25, 10, 10 % на 2, 3, 4, 5-й день терапии соответственно в первой группе. При оценке выраженности клинических проявлений ОРВИ по анализу — снижение баллов по шкале ВАШ на 14, 55, 4, 5 % на 2, 3, 4, 5-й день терапии соответственно во второй группе. Полученные результаты свидетельствуют об эффективности лечения ОРВИ с использованием энисамия йодида. Длительность симптомов общей интоксикации и лихорадки при различных схемах лечения представлена в табл. 1.
У пациентов группы 1 осложнения были выявлены у одного человека, у пациентов группы 2 — у пяти человек. Всем пациентам с выявленными осложнениями была проведена соответствующая диагнозу этиотропная терапия. Результаты с аналогичным клиническим эффектом были зарегистрированы в исследовании М. Л. Науменко с соавторами при лечении ОРВИ у больных с бронхиальной астмой препаратом энисамия йодид [21].
Выявленные до начала терапии ОРВИ нарушения клеточных и гуморальных факторов иммунитета выражались в дисфункциях со стороны нейтрофильных гранулоцитов, иммуноглобулинов периферической крови. Возможной причиной дисбаланса иммуноглобулинов является напряженность функционирования иммунной системы, связанная с наличием очага воспалительного процесса.
На 5-й день терапии в первой группе пациентов зарегистрированы достоверные положительные изменения иммунологических показателей периферической крови: восстановление количественного и субпопуляционного состава лейкоцитов; повышение относительного количества клеток с фенотипом CD3+ , относительного и абсолютного количества CD4+ ; восстановление количества CD3 — CD16+ , CD3 — CD16+ ; снижение до уровня физиологической нормы CD3+HLA-DR+-клеток. На момент проведения контрольного исследования в группе 1 зарегистрированы: нормализация общего числа лейкоцитов и абсолютного количества нейтрофильных гранулоцитов; усиление их фагоцитарных возможностей; увеличение функционального резерва; восстановление биоцидной функции нейтрофильных гранулоцитов и моноцитов в НСТ-тесте, функционального резерва фагоцитов, содержания в сыворотке периферической крови IgA, Ig М, IgG (табл. 2).
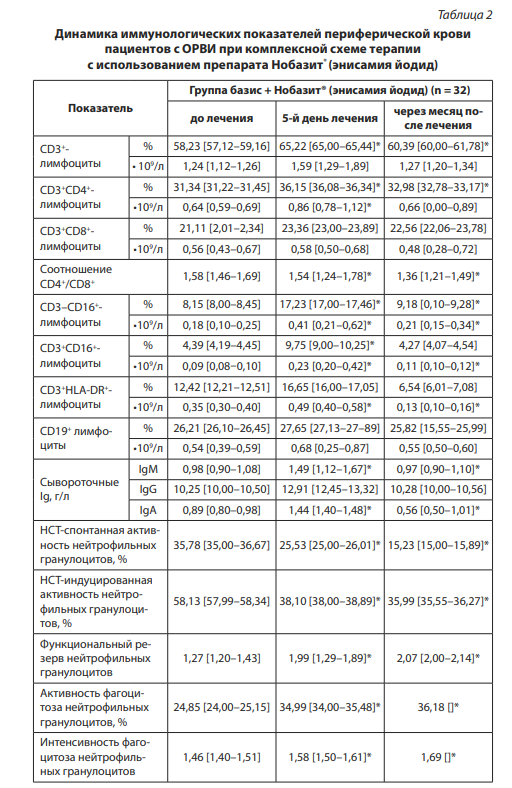
Примечание: * приведены достоверные различия между группами 1, 2, р < 0,05. ИФН — интерферон; CD — кластеры дифференцировки; НСТ — нитросиний тетразолий.
Таким образом, применение препарата Нобазит® (энисамия йодид) усиливает местные защитные реакции, повышая функциональный статус нейтрофильных гранулоцитов периферической крови, усиливает активность гуморальных факторов.
Было изучено содержание CD95+ нейтрофильных гранулоцитов периферической крови (см. рисунок).
При анализе динамики экспрессии поверхностных рецепторов апоптоза на нейтрофильных гранулоцитах было выявлено их достоверное снижение при ОРВИ по сравнению с группой здоровых. Повышенный уровень готовности клеток к апоптозу после лечения препаратом Нобазит® (энисамия йодид), по-видимому, связан со способностью препарата протектировать развитие апоптоза нейтрофилов что, вероятно, приводит к активизации макрофагов, связыванию тромбоспондина, белка, присутствующего в зоне воспаления, способствуя снижению степени проявления воспалительных явлений [5].
Анализ интерферонового статуса представлен в табл. 2. Сывороточные уровни интерферона α (спонтанного и индуцированного) и γ (спонтанного и индуцированного) на 5-й день лечения были статистически значимо выше у пациентов первой группы по сравнению со второй (p < 0,005).
Нормализация сывороточной, спонтанной индуцированной продукции интерферонов α и γ произошло на 5-й день в группе 1, где пациенты получали комплексную терапию ОРВИ с использованием препарата Нобазит® (энисамия йодид) на 5-й день терапии.
Анализ результатов выявил клинико-иммунологическую эффективность использования препарата Нобазит® (энисамия йодид), применение которого в комплексной терапии ОРВИ уменьшает клинические проявления вирусной интоксикации, способствует сокращению продолжительности заболевания, характеризуется хорошей переносимостью: побочных явлений у пациентов не отмечено.
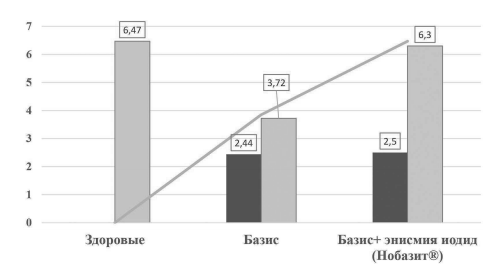
Показатели CD95+ нейтрофильных гранулоцитов периферической крови пациентов с ОРВИ при комплексной схеме терапии с использованием препарата энисамия йодид (Нобазит®) на 5-й день лечения и через месяц после окончания терапии Примечание: приведены достоверные различия между группами, р < 0,05.
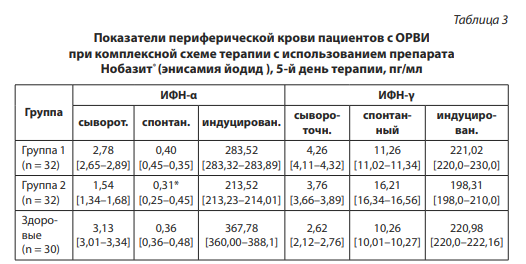
Примечание: * приведены достоверные различия между группами 1, 2, контрольной, р < 0,05. ИФН — интерферон.
ВЫВОДЫ
1. Препарат Нобазит® (энисамия йодид) является современным и высокоэффективным средством для лечения гриппа и острых респираторных вирусных инфекций, достоверно снижает продолжительность лихорадочного синдрома, першения в горле и кашля.
2. Комплексная терапия с использованием препарата Нобазит® (энисамия йодид) стимулирует и нормализует лимфоцитарный рецепторный пейзаж, функциональную активность фагоцитов периферической крови, что проявляется в нормализации абсолютного и относительного количества нейтрофилов, восстановлении потенциала реакций НСТ-теста нейтрофилов, повышении функционального резерва, усилении поглотительных способностей и фагоцитарного числа нейтрофилов.
Конфликт интересов
Автор заявляет об отсутствии конфликта интересов.
Confl ict of interest
The author declares that there is no confl ict of interest.


