Ревматологам часто приходится сталкиваться в своей практике с таким клиническим симптомом, как геморрагическая сыпь. Существует множество причин для возникновения подобных морфологических кожных элементов, поэтому диагностический поиск в отдельных случаях достаточно сложен.
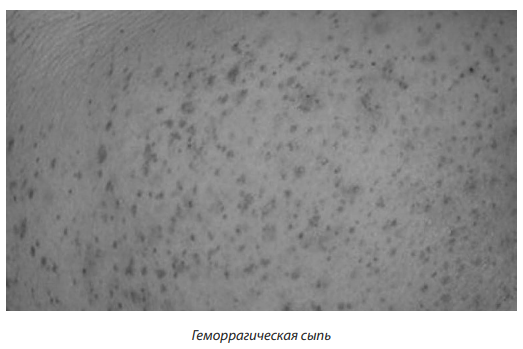
Геморрагическая сыпь (пурпура) — окрашивание кожи или слизистых за счет выхода эритроцитов из сосудов, обычно капилляров. Если экстравазаты очень малы, их называют петехиями, если их диаметр превышает 3 мм — экхимозами. Если пурпура вызвана диапедезом эритроцитов через невоспаленные стенки сосудов, как бывает в случаях, когда пурпура является следствием снижения числа или нарушения функции тромбоцитов, изменениями в системе гемостаза или патологией сосудистой стенки (цинга, амилоидоз), то элементы пурпуры не поддаются пальпации и в этом случае по осязательным ощущениям их нельзя отличить от нормальной кожи. Если пурпура обусловлена воспалительным разрушением стенок сосудов, то фибриноидный некроз стенок сосудов и периваскулярная лейкоцитарная инфильтрация ощущаются в виде уплотнения или бугристости ткани по ходу сосуда. Такая пальпируемая пурпура обычно сопровождает васкулиты. При дальнейшем нарастании воспалительных явлений на фоне сливной пурпуры и экхимозов могут формироваться геморрагические пузыри, оставляющие после вскрытия болезненные эрозии и язвы [1].
Наиболее широко распространенное заболевание из группы системных аутоиммунных васкулитов — геморрагический васкулит (болезнь Шенлейна-Геноха), встречающееся чаще у детей и лиц молодого возраста после острых вирусных и бактериальных (чаще стрептококковых) инфекций, профилактических прививок, переохлаждения, при лекарственной непереносимости. Причиной васкулита является отложение иммунных комплексов, содержащих IgA, в стенке сосуда, что приводит к воспалительным изменениям и последующему повышению проницаемости сосудов. Заболевание складывается из кожного геморрагического синдрома, поражения суставов, абдоминального и почечного синдромов. К проявлению кожного синдрома относят петехиальную сыпь и/или пальпируемую пурпуру, иногда в сочетании с эритематозными пятнами, папулами, пузырьками, которые могут сопровождаться зудом. Распределение кожного процесса симметричное с преимущественной локализацией в дистальных отделах нижних конечностей, с постепенным распространением вверх на бедра и ягодицы. Обычно через несколько дней высыпания бледнеют, приобретают бурую окраску, а затем исчезают. Наиболее часто при болезни Шенлейна-Геноха в патологический процесс вовлекаются крупные суставы нижних конечностей, реже — локтевые и лучезапястные суставы. Как правило, сразу поражается несколько суставов, длительность суставного синдрома редко превышает неделю. Абдоминальный синдром наблюдается у двух третей больных и проявляется спастическими болями в животе, тошнотой, рвотой, редко — желудочно-кишечным кровотечением. Боль обычно локализуется вокруг пупка, но нередко в других отделах живота, симулируя аппендицит, холецистит, панкреатит. Периоды сильной боли могут чередоваться с совершенно безболевыми промежутками. Поражение почек протекает по типу острого или хронического диффузного гломерулонефрита с микро- или макрогематурией, протеинурией, цилиндрурией. В большинстве случаев течение почечного процесса благоприятное (проявления почечного синдрома исчезают через несколько недель или месяцев), но при устойчивой гематурии и протеинурии может развиваться хроническая почечная недостаточность. Лабораторные нарушения при геморрагическом васкулите неспецифичны. У детей в 30 % случаев наблюдается увеличение титров АСЛО. Важным признаком, позволяющим заподозрить заболевание, является увеличение концентрации Ig А в сыворотке крови [2, 3].
Дифференциальная диагностика геморрагического васкулита проводится с другими аутоиммунными заболеваниями (системными васкулитами и заболеваниями соединительной ткани). Поражение кожи по типу пальпируемой пурпуры часто встречается при АНЦА-ассоциированных васкулитах, узелковом полиартериите, криоглобулинемическом васкулите, антифосфолипидном синдроме.
В процессе дифференциальной диагностики васкулитов часто допускаются ошибки вследствие сходности клинической картины. Конституциональные синдромы (лихорадка, похудение, артралгии, миалгии) характерны для всех форм васкулитов. Поражение кожи и слизистых оболочек (ливедо, дигитальные инфаркты, язвы, узелки) развивается при узелковом полиартериите, синдроме Чарджа — Стросса, гранулематозе Вегенера. Пальпируемая пурпура возникает при любой форме васкулита, за исключением гигантоклеточного артериита и артериита Такаясу. Недеструктивный олигоартрит возникает при узелковом полиартериите, гранулематозе Вегенера, синдроме Чарджа — Стросса, пурпуре Шенлейна-Геноха. Множественный мононеврит — патологический процесс при узелковом полиартериите, криоглобулинемическом васкулите, гранулематозе вегенера, синдроме Чарджа — Стросса. Ишемическое поражение почек возникает при узелковом полиартериите, артериите Такаясу. Гломерулонефрит характерен для микроскопического полиангиита, гранулематоза Вегенера, криоглобулинемического васкулита, синдрома Чарджа — Стросса, пурпуры Шенлейна-Геноха. Поражение верхних дыхательных путей, легких развивается при гранулематозе Вегенера, реже — при микроскопическом полиангиите и синдроме Чарджа — Стросса. Боли в животе на разных этапах заболевания возникают при узелковом полиартериите, пурпуре ШенлейнаГеноха, АНЦА-ассоциированных васкулитах. Явления орхита характерны для больных узелковым полиартериитом, пурпурой Шенлейна — Геноха, гранулематозом Вегенера [4].
Диагностика васкулитов основана на детальном клиническом обследовании, позволяющем уточнить характер поражения внутренних органов и исключить другие сходные по клиническим проявлениям заболевания, на оценке клинико-лабораторной активности васкулита, фазы и течения заболевания, степени повреждения органов и систем, на выполнении необходимых для подтверждения диагноза инструментальных, морфологических и лабораторных исследований, на наличии у больного определенных классификационных критериев.
В последнее время, в эру молекулярной диагностики, во всем мире и, в частности, в ревматологическом сообществе возрос интерес к группе аутовоспалительных заболеваний человека. Аутовоспалительные заболевания человека — гетерогенная группа редких, генетически детерминированных состояний, характеризующихся непровоцируемыми приступами воспаления и проявляющихся лихорадкой и клинической симптоматикой, напоминающих ревматическую, при отсутствии аутоиммунных или инфекционных причин. Кроме схожести клинических проявлений, известны случаи ассоциации ревматических и аутовоспалительных заболеваний [5].
Аутовоспалительные синдромы обладают рядом общих патогенетических черт. Причина большинства синдромов — наличие одного мутантного гена. Заболевания встречаются преимущественно в определенных этнических группах. Основное звено патогенеза — гиперактивация систем естественного (антигеннеспецифического) иммунитета. Ведущий медиатор воспаления — ИЛ-1β. Данная группа заболеваний характеризуется эпизодами лихорадки с воспалением серозных, синовиальных оболочек, разнообразной сыпью, высокими лабораторными показателями активности воспаления, возможным развитием амилоидоза.
Семейная средиземноморская лихорадка (ССЛ) — наиболее распространенное заболевание из группы синдромов, называемых аутовоспалительными наследственными периодическими лихорадками. Заболевание встречается преимущественно в определенных этнических группах, относящихся к народам средиземноморского бассейна: у евреев-сефардов, арабов, турок, армян. ССЛ является аутосомно-рецессивным заболеванием. В основе развития ССЛ лежит наличие мутантного гена MEFV (MEditerraenian Fe Ver), расположенного на коротком плече 16-й пары хромосом. В настоящее время известно около 100 мутаций этого гена.
Дебют заболевания почти у 90 % пациентов приходится на возраст до 20 лет. Классическим проявлением ССЛ являются повторные острые (длительностью в среднем от 6 ч до трех суток с интервалами между атаками 3–4 недели) эпизоды лихорадки в сочетании с болевым синдромом: абдоминальными болями (асептический перитонит); торакалгией (плеврит); артритами; а также рожеподобной эритемой кожи (эризипелоидоподобная сыпь на голенях и стопах); повышением уровня неспецифических маркеров острофазного воспаления (СОЭ, СРБ, лейкоциты). Частыми, но непостоянными симптомами являются также миалгии, мигренеподобные головные боли, перикардит, спленомегалия, орхит (отек и болезненность мошонки), а также некоторые ассоциированные васкулиты [6].
В то же время необходимо помнить, что выраженность и сочетание симптомов могут быть различными. Длительность и характер атаки (абдоминальный, плевральный, артритический варианты) у одного и того же больного могут различаться. Период времени между атаками может составлять от нескольких дней до нескольких лет. Наиболее частым симптомом является боль в животе, которая при значительной интенсивности дает картину «острого» живота. В связи с этим пациенты часто подвергаются неоправданным хирургическим вмешательствам. У части пациентов интенсивность абдоминальной боли умеренная или легкая, а продолжительность болевого синдрома составляет от 1 ч до 14 суток. Характерным проявлением ССЛ является спленомегалия, которая возникает в результате хронического воспаления и гиперплазии пульпы. Артрит чаще проявляется моно- или олигоартикулярным поражением крупных суставов нижних или (реже) верхних конечностей, хотя встречается и полиартритический вариант. Продолжительность артрита во время приступа несколько больше, чем других проявлений ССЛ, и составляет в среднем 7 дней. При ССЛ наблюдаются разнообразные кожные проявления, из которых наиболее характерна эризипелоидная эритема, также наблюдаются уртикарные, герпетиформные, псориазоподобные высыпания. Подтверждена более высокая частота встречаемости системных васкулитов (геморрагической пурпуры Шенлейна-Геноха, узелкового полиартериита, болезни Бехчета) у больных ССЛ, что иллюстрирует связь аутовоспалительных заболеваний с ревматической патологией. Типичное, но достаточно редкое проявление ССЛ у пациентов мужского пола — орхит. Во время приступа отмечается повышение острофазовых показателей (СОЭ, СРБ, нейтрофильный лейкоцитоз), также может быть микрогематурия и небольшая протеинурия. Основным осложнением ССЛ является АА-амилоидоз [7, 8].
Диагноз ССЛ основывается в первую очередь на клинических данных. Следует принимать во внимание национальность пациента, наследственность. Также определенное значение в диагностике ССЛ имеет молекулярно-генетическое типирование мутаций MEFV. При этом отсутствие мутаций не исключает диагноз, так как не все патогенные мутации известны на сегодняшний день. Поэтому отрицательный генетический анализ не исключает диагноз ССЛ. Результаты типирования мутаций гена MEFV не входят ни в одни из предложенных диагностических критериев [9, 10].
В настоящее время используются общепринятые критерии Тель-Хашомера (Tel-Hashomer). Эти критерии приведены в таблице. Для постановки диагноза ССЛ необходимо соответствие ≥1 большим критериям, или ≥2 малым критериям, или 1 большому + ≥5 поддерживающим критериям, или 1 малому + ≥4 поддерживающим критериям из числа первых 5.

Типичная атака определяется как рецидивирующая (+3 сходных эпизода), фебрильная (ректальная температура ≥38,0 °С) и короткая (продолжительностью от 12 ч до 3 дней). Неполная атака определяется как болевая и рецидивирующая атака, отличающаяся от типичной по одному или двум из следующих признаков: 1) температура — нормальная или ниже 38,0 °С; 2) атака длиннее или короче, чем специфическая (но не менее 6 ч и не более 1 нед.); 3) отсутствуют перитонеальные симптомы во время абдоминальной атаки; 4) абдоминальная боль носит локализованный характер; 5) артриты возникают в «неспецифических» суставах [4, 5].
Больной А, 23 лет, поступил в экстренном порядке (по СМП) в ревматологическое отделение ГКБ № 15 21.02.2017 с жалобами на подъем температуры до 38,5 °С, на боли, отечность кистей, боли в коленных, левом локтевом суставах, геморрагические высыпания на нижних и верхних конечностях, туловище, потливость, общую слабость. Из анамнеза жизни: вредные привычки (курение, алкоголь), операции, травмы, контакт с инфекционными больными — отрицает; национальность — армянин; не работает. Также из анамнеза известно, что в декабре 2011 г. впервые обратился к терапевту по месту жительства с жалобами на боли в эпигастрии. По данным ЭГДС: поверхностный гастрит (биопсия: H. pylori не выявлен, гиперплазия клеток покровно-мышечного эпителия с кишечной метаплазией, клеток злокачественной опухоли в пределах исследуемого материала не обнаружено). Выставлен диагноз «хронический гастрит». В марте 2012 г. — вновь боли в эпигастрии, стационарное лечение в ГКБ № 50 с диагнозом «острый мезаденит». По данным УЗИ органов брюшной полости: признаки спленомегалии, увеличение внутрибрюшных л/у. Клинический анализ крови: Hb — 125 г/л, лейкоциты — 5,3х109/л, тромбоциты — 304х109/л, СОЭ — 34 мм/ч. Общий анализ мочи: белок — 0,55 г/л, лейкоциты 7–9 в п/зр., эритроциты — единичные в п/зр.; ЭГДС: гастродуоденит. В период с 2012 г. — ежегодные приступы болей в животе, сопровождающиеся лихорадкой, при этом болевой синдром и лихорадка купировались самостоятельно или после приема анальгетиков. В апреле 2017 г. — боли в эпигастрии, стационарное лечение в хирургическом отделении с диагнозом: хронический панкреатит, обострение, спленомегалия, лимфаденопатия. Общий анализ мочи: белок — отр., в биохимическом анализе крови — увеличение СРБ, в клиническом анализе крови — увеличение СОЭ. КТ органов брюшной полости: спленомегалия, увеличенные мезентериальные и парааортальные л/у, мелкий конкремент в желчном пузыре. Проводилась спазмолитическая терапия с положительной динамикой. Консультирован в клинике гематологии и клеточной терапии им. А. А. Максимова, выставлен диагноз: реконвалесценция цитомегаловирусной инфекции, вирус Эпштейн-Барра, спленомегалия. В ФГБУ Гематологический научный центр проведена трепанобиопсия, результат: вторичные изменения; клетки мутации Jak2 не обнаружены. Последние три года — частые приступы межреберной невралгии, купирующиеся самостоятельно. 15.02.2017 — эпизод межреберной невралгии (боли при глубоком вдохе). 17.02.2017 повышение температуры тела до 38,5 °С, боли в правом локтевом суставе, далее присоединились боли в правом коленном суставе, появилась геморрагическая сыпь на голенях, далее — боли в левом локтевом, левом коленном суставах, диффузный отек кистей, далее — геморрагические высыпания на верхних конечностях. Самостоятельно принимал нестероидные противовоспалительные средства с незначительным эффектом в виде снижения температура тела, исчезновения боли в правом локтевом суставе. На следующий день вновь подъем температуры тела до 38,5 °С, что в сочетании с суставным синдромом послужило причиной госпитализации в ревматологическое отделение ГКБ № 5 им. О. М. Филатова для уточнения диагноза и лечения.
Состояние при поступлении средней тяжести. Температура 37,0 °С. Рост 1,73 м. Вес 73 кг. ИМТ 24,39 кг/м2 . Конституция нормостеническая. На коже верхних, нижних конечностей, туловища отмечаются множественные геморрагические высыпания: петехии, экхимозы, «пальпируемая пурпура». Слизистые оболочки без видимых патологических изменений. Дыхание через нос свободное. Перкуторный звук легочный. В легких дыхание везикулярное, хрипы не выслушиваются, ЧДД 20 в мин. SaO2 — 99 % на воздухе. Границы сердца не расширены. Тоны сердца приглушены, ритм правильный. ЧСС 100 уд./мин. АД 160/80 мм рт. ст. Живот при пальпации мягкий, безболезненный. Печень у края реберной дуги. Селезенка увеличена. Физиологические отправления не нарушены. Симптом поколачивания по поясничной области отрицательный с обеих сторон. Опорно-двигательная система: диффузный отек кистей, положительный симптом поперечного сжатия кистей. Движения в лучезапястных, плечевых суставах в полном объеме, безболезненные. Дефигурация левого локтевого сустава за счет экссудативных изменений, неполное разгибание, боли при движении. Дефигурация коленных суставов за счет экссудативных изменений, боли при пальпации и движениях. Неврологический статус: когнитивных нарушений нет. Менингеальные знаки: нет. Черепные нервы: без выпадений. Двигательная сфера: парезов нет. Мышечный тонус, рефлекторная сфера: D=S. Патологические стопные знаки: нет. Чувствительность: не изменена. Проба Ромберга: устойчив.
При обследовании: клинический анализ крови (гемоглобин — 124 г/л, лейкоциты — 10,0–109/л, тромбоциты — 378–109/л, СОЭ — 75 мм/ч); биохимический анализ крови — все показатели в пределах нормальных значений; общий анализ мочи — эритроцитурия 45 в п/зр., протеинурия 1 г/л. Анализ мочи по Нечипоренко: лейкоциты 4000 (0–2000 в 1 мл), эритроциты 35 000 (0–1000 в 1 мл), цилиндры — нет (0–1 в камере). РМП, ВИЧ, аHBsAg, аHCV — отрицательно. Коагулологическое исследование: АЧТВ 26,2 (норма 22–32 с), протромбиновое время 16,3 (норма 9,8–12,1 с), волчаночный антикоагулянт не обнаружен. Иммунологический анализ крови: С-РБ 49,5 (0,0–5,0 мг/л), АСЛО 53,0 (0,0–200,0 МЕ/мл), ревматоидный фактор 6,0 (0,0–15,0 МЕ/мл), определение белковых фракций: гамма — глобулины 21,1 (11,1–18,8 %), иммуноглобулины IgG 29,1 (6,8–16,5) г/л, IgM 2,5 (0,4– 2,5 г/л), IgA 2,6 (0,7–3,74 г/л), антитела к двуспиральной ДНК (dsDNA) 17,70 (норма <25,00 МЕ/мл), антитела к ядерным антигенам 0,50 (менее 1 — не обнаружено, от 1 до 1,2 — серая зона; более 1,2 — обнаружено), антитела к кардиолипину IgG (GLP-IgG) 2,60 (норма < 10,00 МЕ/мл), IgМ (GLP-IgM) не обнаружено, антитела к b2 гликопротеину I IgG (b2-GP1-G) 3,60 (норма <5,00 Ед/мл), IgM (b2-GP1-M) не обнаружено, антинейтрофильные антитела (ANCA) к МРО, PR3; антитела к GBM — не обнаружено, криоглобулины — отр. Иммунохимический анализ крови и мочи: в сыворотке крови — уровень поликлональных IgG, IgA, IgM, IgD в пределах нормы. Повышен уровень бета-2микроглобулина в сыворотке крови и в моче. Моноклональная секреция не выявлена. Бактериологический анализ крови: роста облигатно-анаэробной, факультативно-анаэробной и аэробной микрофлоры нет. Бактериологический анализ мочи: рост микрофлоры не выявлен. Бактериологический анализ слизистой зева: этиологически значимого роста нет. Анализ синовиальной жидкости: ураты, пирофосфаты кальция не обнаружены.
ЭКГ: ритм неправильный, ЧСС 120/мин. Вертикальное положение ЭОС. Синусовая тахикардия. ЭХО-КГ: камеры сердца имеют нормальные размеры и сократимость. Утолщения стенок левого желудочка (более 1,1 см в диастолу) не выявлено. Аортальная недостаточность небольшая. Небольшая митральная и трикуспидальная регургитация. Перикард — без патологии. Дуплексное сканирование брахиоцефальных сосудов: гемодинамически значимых препятствий и асимметрии кровотока по парным артериям на момент исследования не выявлено. Компьютерная томография органов грудной клетки: КТ-данных за патологические изменений органов грудной полости не выявлено. УЗИ органов брюшной полости: УЗ-признаки диффузных неспецифических изменений печени, повышенной плотности пузырной желчи, выраженной спленомегалии [площадь 96,0 см2 (норма до 50,0 см2)], увеличения обеих почек с утолщенной паренхимой. Эзофагогастродуоденоскопия: недостаточность кардии. Скользящая аксиальная хиатальная грыжа. Дистальный хронический рефлюкс-эзофагит. Поверхностный гастрит. Колоноскопия: признаки хронического колита. Компьютерная томография с контрастированием аорты и ее ветвей, почечных артерий: данных о патологии брюшного отдела аорты и почечных артерий не выявлено. Количественная регионарная лимфаденопатия. Небольшое количество жидкости в полости малого таза.
В период госпитализации пациент также стал предъявлять жалобы на боли в животе, которые локализовались в эпигастральной области, возникали вне связи с приемом пищи, купировались самостоятельно в течение нескольких часов или после применения анальгетиков. Учитывая наличие геморрагической сыпи, артритов, мочевого синдрома, спастических болей в животе, повышения лабораторных маркеров воспаления, отсутствия клинико-инструментальных данных других системных васкулитов, выставлен диагноз «геморрагический васкулит». С учетом поражения почек назначен Преднизолон 30 мг/сут. На фоне терапии температура нормализовалась, кожные элементы быстро регрессировали, боли в суставах уменьшились, в повторных анализах мочи белок не обнаруживался, сохранялась микрогематурия, однако боли в животе рецидивировали. Также обращала на себя внимание значительная спленомегалия. После более тщательного анализа семейного анамнеза диагноз был дополнен. Учитывая периодически возникающие боли в животе, не связанные с приемом пищи, периодическую лихорадку, национальную принадлежность больного (армянин), указание на наличие периодической болезни у кровных родственников, возраст начала заболевания, спленомегалию, суставной, мочевой синдромы, повышение лабораторных маркеров воспаления (СОЭ, СРБ, лейкоцитоз, фибриноген), выставлен диагноз: «периодическая болезнь (семейная средиземноморская лихорадка), удовлетворяющий критериям Тель-Хашомера». Произведена биопсия слизистой антрального отдела желудка — при окраске Конго рот амилоид не обнаружен. Начато быстрое снижение дозы ГКС, назначен Колхицин. Отмечен хороший эффект после терапии Колхицином: боли в животе не рецидивировали.
Таким образом, этот случай иллюстрирует схожесть клинической симптоматики аутовоспалительных и ревматических заболеваний. Диагноз ставится путем исключения тех заболеваний, которые по своему клиническому течению похожи на одну из форм ССЛ. Точный диагноз очень ответственен, так как терапевтические подходы разные. Аутовоспалительные заболевания сами по себе имеют серьезный прогноз, и для больных с этими заболеваниями своевременно поставленный диагноз и адекватно подобранная терапия являются жизненно важными. Необходимо тщательно анализировать национальную принадлежность, наследственность, анамнез заболевания больного. Следует иметь в виду возможность нетипичного течения аутовоспалительного заболевания («неполные атаки» при ССЛ), а также сочетание с ревматическим заболеванием. В представленном случае отмечались клинические проявления геморрагического васкулита, который достаточно часто наблюдается у больных с аутовоспалительными заболеваниями, и в первую очередь с ССЛ, о чем также следует помнить, когда мы видим молодого пациента с геморрагической сыпью.


