Введение
Первое упоминание о компрессии общего малоберцового нерва (ОМН) на уровне головки малоберцовой кости принадлежит H.W. Woltman. В 1929 г. он описал 7 случаев возникновения невропатии ОМН у людей, длительно сидящих в позе «нога на ногу» [1]. Позже эту патологию в 1934 г. французские клиницисты Guillain G., de Seze S., Blondin-Walter M. оценили как «профессиональный паралич копальщиков луковиц тюльпанов» [2]. В зарубежной литературе canalis musculoperoneus superior чаще именуют фибулярным [3]. Фибулярный туннельный синдром (ФТС) считается наиболее распространенным видом невропатии нижних конечностей и 3-м по частоте туннельным синдромом (составляет 10–15 % всех туннельных невропатий) [4, 5]. Актуальность проблемы диагностики и лечения СФК подчеркивают данные регистра травм в Германии, согласно которому в 1,8 % случаев травм нижних конечностей развивается поражение периферических нервов, при этом более половины случаев (56 %) составляет невропатия ОМН [6].
Этиология
Развитию ФТС способствуют врожденная или приобретенная узость канала, длительная микротравматизация нервных стволов, снижение толерантности аксонов к механическому сдавлению и ишемии [7]. Крыша фибулярного канала образуется началом m. peroneus longus и межмышечной перегородкой, верхняя порция арки прикрепляется к головке малоберцовой кости, а нижняя — к ее боковой поверхности (рис. 1–3).
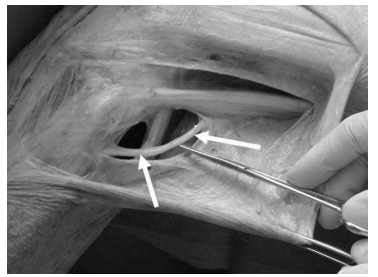
Рис. 1. Общий малоберцовый нерв [8]
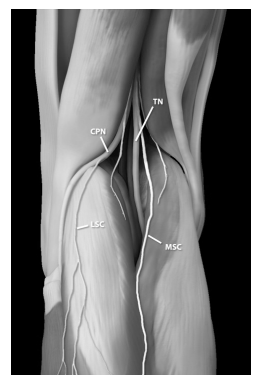
Рис. 2. 3D-рендеринг заднелатеральной стороны колена, демонстрирующий разветвление седалищного нерва на общий малоберцовый (CPN) и большеберцовый нервы (TN), а также вклады латерального икроножного (LSC) и медиального икроножного (MSC) нервов [9]
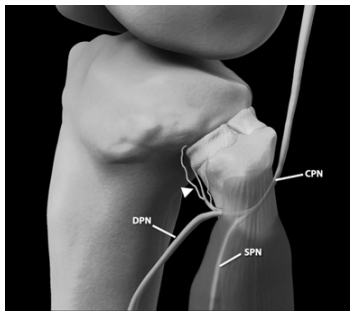
Рис. 3. Трехмерное изображение боковой поверхности колена, демонстрирующее ход общего малоберцового нерва (СPN) ниже проксимальной головки длинной малоберцовой мышцы в малоберцовом туннеле. Общий малоберцовый нерв разветвляется на поверхностный малоберцовый нерв (SPN) и глубокий малоберцовый нерв (DPN), а также дает ответвления к проксимальному межберцовому суставу (стрелка) [9].
Невропатия ОМН в области головки малоберцовой кости может быть вызвана сдавлением различными субстратами: уплотненной фасцией, отломками кости при травме (перелом проксимального отдела малоберцовой кости, перелом большеберцовой кости, вывих в коленном суставе и др.), неправильно наложенной гипсовой лонгетой и др. [5, 10]. Преимущественно страдают лица, работающие на корточках и на коленях (сборщики мебели, корнеплодов, винограда, укладчики плитки и паркета, чистильщики обуви). Невропатия ОМН часто встречается у спортсменов и профессиональных барабанщиков [11]. Отмечено, что повторяющееся сгибательное и разгибательное движение в коленном суставе (КС) с дополнительным отягощением в некоторых случаях может привести к компрессии ОМН на уровне входа в m. peroneus longus за счет напряжения фибулярной арки [12].
В роли этиотропного и провоцирующего фактора могут также выступать продолжительная поза «нога на ногу» (у анорексичных фотомоделей), пребывание в высоком кресле со свободно свисающими ногами, сон в неудобной позе (согнутая в КС нога, свисающая через край кровати нога, сон сидя), гипсовая повязка [13, 14]. К более редким причинам ФТС принадлежат системные заболевания, сопровождающиеся пролиферацией соединительной ткани (склеродермия, подагра, ревматоидный артрит, полимиозит), метаболические нарушения (сахарный диабет), тяжелые инфекции, интоксикации (алкоголизм, наркомания) и местные опухолевые процессы (костей и мягких тканей) [15, 16, 17]. Сахарный диабет ведет к ФТС, поскольку отложение сорбитола в ОМН вызывает отек нервной ткани, приводящий к компрессии [18]. ФТС из-за костных наростов также часто отмечалась в многочисленных отчетах о случаях. 2 случая были связаны с остеохондромами головки малоберцовой кости, вызывающими захват ОМН, 2 из которых были устранены с помощью удаления опухоли. Более редкие случаи разрастания костей включают мелореостоз, гиперостоза кости, сесамовидная кость в заднебоковом колене, вызывающая компрессию ОМН, которая требовала лечения с хирургическим удалением костных поражений [19].
Клиническая картина
ФТС характеризуется преимущественно острым (от 1 до 24 часов), реже — подострым (менее чем у 20 % пациентов — от 2 до 10 суток) [20]. У пациентов с невропатией ОМН можно выделить паралитическую, болевую и перемежающуюся формы заболевания [5]. При классической форме ФТС является наличие нарушений чувствительности и двигательной функции в сочетании с положительным симптомом Тинеля, вызываемым на уровне головки малоберцовой кости, облегчает постановку диагноза [11, 21]. Наблюдаются парестезии по наружной поверхности голени и стопы. Интенсивный болевой синдром при ФТС (ввиду малого содержания тонких немиелинизированных «болевых» волокон) нехарактерен, поэтому в начальной стадии заболевания у пациентов отсутствуют настороженность и беспокойство по поводу сенсорных нарушений, и они нередко оказываются перед фактом уже развившегося пареза. Даже в тех случаях, когда ФТС сопутствует болевой синдром (<20 %), парез способствует существенному уменьшению или исчезновению боли, и пациенты длительное время игнорируют двигательный дефект [22]. ФТС проявляется различными симптомами нарушения иннервации мышц переднего и латерального лож голени, а также дорсальной стороны стопы [23]. Наиболее часто у пациентов наблюдается грубый парез при сгибании в голеностопном суставе (ГС) и при отведении стопы, разгибании пальцев, вплоть до плегии, изменение походки по типу петушиной (степпаж), в сочетании с гипестезией тыльной поверхности стопы [4, 15]. M. Van Langenhove et. al. (1989) обследовали 303 больных с плегией при сгибании в ГС, из которых поражение ОМН диагностировано у 31 %, радикулопатия на уровне позвонка L5 — у 19,7 % [5]. В каждом 10-м случае нарушения выявляются с 2 сторон. По данным Кипервас И.П. (2010), анализ лечения 184 пациентов с ишиасом и параличом стопы показал, что 1/6 лиц имели ФТС [24].
Важным дифференциальным критерием диагностики у таких больных оказывается симптом Тинеля на уровне головки малоберцовой кости [25]. Он становится практически единственным реальным основанием для верификации ФТС. В 2011 г. Zywiel M.G. et. al описали клинические критерии перонеальной дисфункции [26].
1. Боль или чувствительные нарушения при сгибании и разгибании ноги в КС.
2. Иррадиацией боли по латеральной поверхности голени и тыльной стороны стопы.
3. Преходящий паттерн симптомов, возникающих при движении.
4. Положительный симптом Тинеля на уровне головки малоберцовой кости.
Важным критерием, необходимым для выявления перемежающейся формы ФТС, является тест повторного подошвенного сгибания, предложенный K. Kim et. al (2015). Во время выполнения тыльного сгибания и подошвенного разгибания за счет сокращения m. peroneus longus и m. soleus происходит напряжение фибулярной арки, что приводит к развитию симптоматики невропатии ОМН [25]. Методика теста выглядит так: пациент находится в положении сидя с разогнутым КС и выполняет как можно более полные по амплитуде подошвенные сгибания и разгибания ГС в течение 2 мин; тест считается положительным при возникновении боли в пораженной области. В среднем симптомы появляются через 57,4 сек. (диапазон — 14–120 сек.) [11]. Клинически оценку сенсорного и моторного неврологического дефицита невропатии ОМН проводят по шкале British Medical Research Council Scale (BMRCS) [3, 27].
Диагностика
Использование электронейромиографии (ЭНМГ) в диагностике ФТС позволяет выявить степень нарушения проводимости по нервным стволам, но не определяет причину этого нарушения [28, 29, 30]. Нужно помнить, что ценность ЭНМГ при перемежающейся форме невропатии ОМН весьма низкая [11]. По данным D. Morimoto et. al (2015), в наблюдении из 22 лиц подобным типом невропатии у 13 (59,1 %) пациентов не было выявлено изменений по ЭНМГ [31]. А по данным Башлачева М. Г. и соавт. (2021) ЭНМГ не выявила отклонений от нормы у 50 % лиц [11]. Для планирования вида и объема оперативного вмешательства требуется проведение дополнительных инструментальных методов исследования (УЗИ или МРТ) с целью верификации новообразований и др. [32, 33, 34]. Чувствительность УЗИ в диагностике невропатии ОМН составляет 93 % по сравнению с 67 % для МРТ при аналогичной специфичности (86 %) [35]. Увеличение ОМН при УЗИ является признаком при нервных расстройствах, а измерение площади поперечного сечения ОМН является наиболее широко признанным и надежным методом диагностики нервных расстройств [35]. Критерием отека ОМН в фибулярном канале, по мнению M.A. Bedewi et. Al. (2018), является увеличение площади его поперечного сечения более 12,1 кв. мм [36]. МРТ позволяют визуализировать ход и морфологию ОМН с состоянием окружающих тканей и костных структур, которые могут вызывать сдавление: отек мягких тканей и ОМН, тендинит, синовиит, объемные образования и др. [37, 38, 39]. При травматической невропатии ОМН требуется консультация травматолога-ортопеда, по показаниям — рентгенография КС, ГС и костей голени; МРТ или УЗИ мягких тканей голени [40, 41, 42]. В отдельных случаях могут применяться диагностические блокады ОМН под УЗИ-навигацией [43, 44, 45]. Дифференциальную диагностику проводят со спинальным стенозом, радикулопатией, полинейропатией, объемными образованиями ОМН (шваннома, ганлион), наследственной рецидивирующей невропатией, болезнью Шарко-Мари-Тута, синдромом перонеальной мышечной атрофии, боковым амиотрофическим склерозом, другими мононевропатиями нижних конечностей, опухолями головного мозга и позвоночника [46, 47, 48].
Лечение
Консервативное лечение. В настоящее время не существует эффективной консервативной терапии СФК. В качестве консервативных методов коррекции пареза разгибателей стопы и улучшения походки могут быть эффективны ортезы и лечебная гимнастика, а также чрескожная электрическая стимуляция паретичных мышц [49, 50]. Антиконвульсанты, антидепрессанты, сосудистые, антиоксидантны, противовоспалительные и антихолинэстеразные препараты, физиотерапия (ультразвук с гидрокортизоном, СМТ-терапия, магнитотерапия, воздействие на биологически активные точки лазеротерапией, электроакупунктурой, сегментарный массаж используются при данном виде заболевания [51, 52, 53]. Альтернативное лечение, которое следует рассмотреть перед хирургическим вмешательством, включает гидродиссекцию под УЗИ-контролем [19]. Лечение включает инъекцию раствора (местные анестетики, глюкокортикостероиды, плазму и декстрозу) вокруг ОМН, чтобы уменьшить давление со стороны окружающих структур. Основными функциями этого лечения являются устранение спаек мягких тканей, которые вызывают защемление, и восстановление функции ОМН.
Хирургическое лечение
Выполнение операции проводится с применением микрохирургической техники, производится разрез кожи длиной 8–12 см от проекции нижней части сухожилия m. biceps femoris до области проекции верхних отделов m. peroneus longus [54]. Обнаруживается ОМН под сухожилием m. biceps femoris и, двигаясь дистально, проводится декомпрессию ОМН (невролиз). Типичными причинами компрессии ОМН были: уплотненная поверхностная фасция, покрывающая ОМН в проекции головки малоберцовой кости, и уплотненная фасция m. peroneus longus в месте входа ОМН в толщу данной мышцы. Эти структуры последовательно рассекают с целью полной декомпрессии ОМН [55].
Результаты исследований показали, что эффективность хирургической декомпрессии существенно выше в первые 3 мес. заболевания, далее ее эффективность постепенно снижается и становится незначительной через 12 мес. после начала заболевания [5]. Ramanan M. и Chandran K.N. также показали, что результаты вмешательств в срок >12 мес. от начала заболевания хуже, чем при операциях в более ранние сроки [2]. Согласно общепринятому мнению, хирургическое вмешательство следует проводить (не учитывая случаи острой травмы по типу разрыва нерва или сдавления ОМН гематомой) при неэффективности консервативной терапии в течение 3–6 мес. [5]. Maalla R. et. al. демонстрируют наиболее радикальный подход к лечению данной патологии [56]. Они предлагают выполнять декомпрессию ОМН в максимально короткие сроки (сразу после установления диагноза), так как это уменьшает срок восстановления ОМН и позволяет большинству пациентов быстрее вернуться к активной жизни.
Terzis J. K. and Kostas I. (2020) провели ретроспективный анализ 35 пациентов, перенесших микронейролиз и декомпрессию ОМН, привел только к 1 плохому результату, на это указывает неспособность согнуть стопу до 90 градусов [57].
Башлачев М. Г. и соавт. (2021) представили 80 пациентов (31 женщина и 49 мужчин) в возрасте от 18 до 82 лет (средний возраст — 51 год) с ФТС. У 76 пациентов установлено одностороннее поражение, у 4 — двустороннее, было выполнено 84 операции. Паралитическая форма ФТС выявлена в 73 (87 %) случаях оперативных вмешательств, болевая — в 8 (9,5 %), перемежающаяся — в 3 (3,5 %). После хирургического лечения полное восстановление функции ОМН отмечено в 61 из 84 (72,6 %) случаев оперативных вмешательств, частичное восстановление — в 15 (17,9 %). Положительные результаты наблюдались во всех случаях болевой и перемежающейся форм ОМН, а при паралитической форме они отмечались чаще, если операция проводилась в ранние сроки (до 12 мес.) от начала заболевания [5].
Байтингер А. В. (2021) представил результаты лечения 30 пациентов с ФТС. До операции у 14 из 30 пациентов сила m. tibialis anterior и m. extensor digitorum longus была M1, у 16 — М2 (по шкале BMRCS). После хирургического вмешательства у 6 пациентов сила осталась на прежнем уровне М2, у 1 пациента увеличилась до М3, у 23 пациентов — до М4. Уменьшение силы и прогрессирование глубины моторных расстройств не наблюдалось. До операции у 14 из 30 пациентов отсутствовала чувствительность (S0), у 16 — S1. После операции у 1 пациента чувствительность оставалась на прежнем уровне S1, у 6 — увеличилась до S3, у 23 пациентов восстановилась полностью — до S4. Было показано статистически значимое превышение значения медианы по шкале моторного дефицита после операции (Median = 4) над медианой до операции (Median = 2) при критерии Вилкоксона Z = 4,457; p < 0,0001. Также выявлено статистически значимое превышение значение медианы по шкале сенсорного дефицита после операции (Median = 4) над таковой до операции (Median = 1) при критерии Вилкоксона Z = 4,540; p < 0,0001 [3].
В последние годы активно внедряются методики минимально инвазивной хирургии, в том числе эндоскопические, в лечении ФТС [58]. При сохранении болей после операции возможно радиочастотная абляция или крионанальгезия ОМН [59, 60, 61].
Заключение
Несмотря на тот факт, что ФТС известен широкой медицинской общественности > 90 лет, количество пациентов, которым не удалось поставить этот диагноз, не уменьшается. На настоящий момент врачи-клиницисты в большинстве своем не связывают клинические проявления с ФТС, что приводит к диагностическим ошибкам и, как следствие, к неправильной тактике лечения и снижению качества жизни пациентов на продолжительное время. Диагностировать компрессионной невропатии ОМН при наличии у пациента классической клинической картины — с нарушениями чувствительности и двигательной функции, положительным симптомом Тинеля и наличием электрофизиологических отклонений — не составляет труда. Ошибки в диагностике отмечаются при болевой и перемежающейся формах невропатии ОМН. Декомпрессионная операция при ФТС — эффективный и безопасный метод лечения, который следует проводить в ранние сроки заболевания. У пациентов с болевой и перемежающейся формами ФТС операция приводит к полному регрессу симптоматики. При паралитической форме заболевания полное восстановление функции ОМН наблюдается более чем в половине наблюдений и возникает чаще, если операция проводилась в ранние сроки от начала заболевания.
КОНФЛИКТ ИНТЕРЕСОВ
Авторы заявляют об отсутствии конфликта интересов.
CONFLICT OF INTEREST
The authors declare no conflict of interest.


